趋化因子是招募CD8+T细胞的重要因素[4] 。 那TRIB3调控CD8+T细胞的浸润是不是通过趋化因子介导的呢?如果是 , 又是哪一个趋化因子呢?
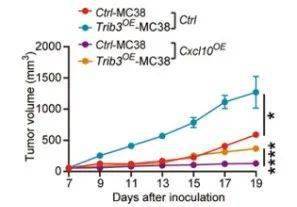
带着这些疑问 , 他们先用荧光微球流式细胞实验(CBA)对多种趋化因子进行了筛选 ,发现CXCL10在Trib3 KD MC38细胞中表达明显增高 , 且CXCL-10的中和性抗体能够有效地抑制CD8+T细胞的迁移。 除此以外 , 他们还建立了CXCL-10/TRIB3双过表达模型(Cxcl10 OE Trib3 OE )进行体内实验 , 也得到了一致的结果 , CXCL10 OE 可以抑制TRIB3 OE 的促肿瘤作用 。
文章图片
体内实验显示过表达CXCL-10可以抑制Trib3 OE 促肿瘤能力
据报道 , STAT1 , NF-κB和CREB均是可以调节CXCL10表达的转录因子[5] 。 他们分别敲低STAT1 , NF-κB和CREB , 发现敲低STAT1后可以逆转Trib3 KD 引起的CXCL-10增高趋势 , 而NF-κB和CREB均不可以 。 进一步实验证明 TRIB3调节STAT1/CXCL-10通路是通过STAT3/EGFR来介导的 。
到此 , 该团队已经明确 , TRIB3-STAT1-CXCL10通路可以重建肿瘤微环境 , 调节CD8+T细胞的浸润 。但是 , 还有一个大问题没有解决:到底什么影响TRIB3的表达?
以往的研究和本研究前面的结果已经表明高糖调节和肥胖可以促进TRIB3的表达 , 所以 , 他们用高糖去处理结直肠癌细胞系 , 发现Trib3的转录水平没有变化 , 但是TRIB3蛋白水平明显增多 。 这个结果也意味着 高糖是通过增加TRIB3蛋白的稳定性来增高其蛋白的表达量 。
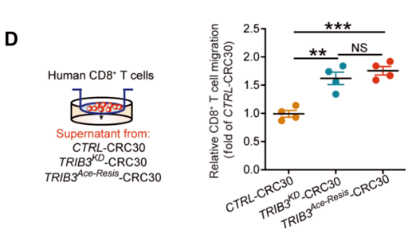
高糖可以给肿瘤细胞提供足够的能量来源 , 并且产生大量的乙酰辅酶A(CoA) , 而CoA又能进一步将蛋白进行乙酰化修饰[8] 。 检测也发现 , 高糖处理能乙酰化修饰TRIB3 。 进一步实验确定了 组蛋白乙酰转移酶P300可以介导TRIB3蛋白的K240位点乙酰化 , 这对于CD8+T细胞的浸润是不利的 。
文章图片
TRIB3 K240位点的乙酰化抑制CD8+T的迁移
既然TRIB3的乙酰化修饰对抗肿瘤免疫具有负面作用 , 那么 , TRIB3乙酰化的拮抗剂是否能够促进抗肿瘤治疗呢?
因此 , 他们联用C646(乙酰化抑制剂)和PD-L1抗体治疗CT26原位结直肠癌 。 结果显示 ,不管是单独使用C646还是PD-L抗体 , 都能够部分限制肿瘤进展 , 而两者联用可以显著增加抗肿瘤疗效 。 机制也和前面的结果一致 , 联合治疗能够增加CD8+T细胞的浸润 , 伴随着TRIB3表达量明显降低 , 而CXCL10 , STAT1和p-STAT1则明显增高 。
文章图片
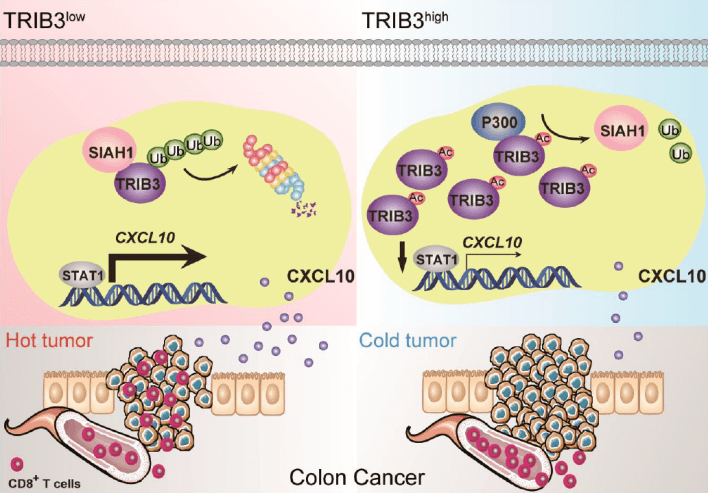
TRIB3影响肿瘤免疫微环境机制示意图
这个研究不仅明晰了肥胖人群易患肿瘤的机制 , 也为未来对于结直肠癌患者的治疗提供了潜在的靶点 。
备注:由于昨天将“协和医学院”写成“协和医院” , 昨晚的推送已经删除

文章图片
。 在征得花教授同意之后 , 今天修改作者单位之后 , 重新推送

文章图片
~
参考文献:
1. The 2018 Nobel Prize in Physiology or Medicine - Press release - NobelPrize.org. https://www.nobelprize.org/prizes/medicine/2018/press-release/.
2. Shang, S. et al. TRIB3 reduces CD8+ T cell infiltration and induces immune evasion by repressing the STAT1-CXCL10 axis in colorectal cancer. Sci. Transl. Med. 14, eabf0992 (2022).
- 大年|多嚼就能少胖!科学家发现咀嚼会增加进食消耗的热量,积少成多不容易胖丨奇点过大年
- 春季多吃葱蒜顺养肝气抗肿瘤
- 手术|安分了十几年的肿瘤突然变大十多倍,到医院一检查,个头比甜瓜还要大
- 饮食|老年人身体素质的提高,科学饮食是关键
- 春季要学会科学饮水
- 冬藏|中医说的“冬藏”,究竟怎么“藏”?
- 食物|春节期间,如何科学选择零食
- 早春全方位调整
- 肿瘤|致敬!院士放弃专利让救命药一盒仅290元
- 春季饮食红枣的妙用之处
