(健康时报采访人员 邱越)2月11日,国家药监局附条件批准了美国辉瑞公司新冠病毒治疗药物奈玛特韦片/利托那韦片组合包装(即Paxlovid)进口注册。这是国内上市的第一款口服新冠药物,也是迄今为止国内上市的第二款新冠治疗药物。
2021年12月8日,国家药品监督管理局应急批准腾盛华创医药技术(北京)有限公司新冠病毒中和抗体联合治疗药物安巴韦单抗注射液(BRII-196)及罗米司韦单抗注射液(BRII-198)注册申请。
国内患者何时能用上新冠特效药呢?2月14日,健康时报采访人员分别联系了辉瑞和腾盛博药。
名称
Paxlovid(奈玛特韦片/利托那韦片组合包装)
安巴韦单抗注射液及罗米司韦单抗注射液
研发单位
辉瑞公司
清华大学、深圳市第三人民医院、腾盛博药合作研发
进口or原研
进口
原研
产品类型
口服小分子
中和抗体
给药方式
每天口服两次,持续5天
静脉注射,只需给药1次
适用人群
成人
成人和青少年(12-17岁,体重≥40kg)
制图:邱越
国内第一个口服新冠药物:上市消息将及时公布据国家药监局介绍,Paxlovid为口服小分子新冠病毒治疗药物,用于治疗成人伴有进展为重症高风险因素的轻至中度新型冠状病毒肺炎(COVID-19)患者,例如伴有高龄、慢性肾脏疾病、糖尿病、心血管疾病、慢性肺病等重症高风险因素的患者。
2月14日,健康时报采访人员从辉瑞公司获悉,目前Paxlovid刚刚获批,具体的上市计划尚不掌握,若想知道药品何时上市、在什么城市的哪些医院落地等信息,还需等待一些时日。有消息将第一时间公布。
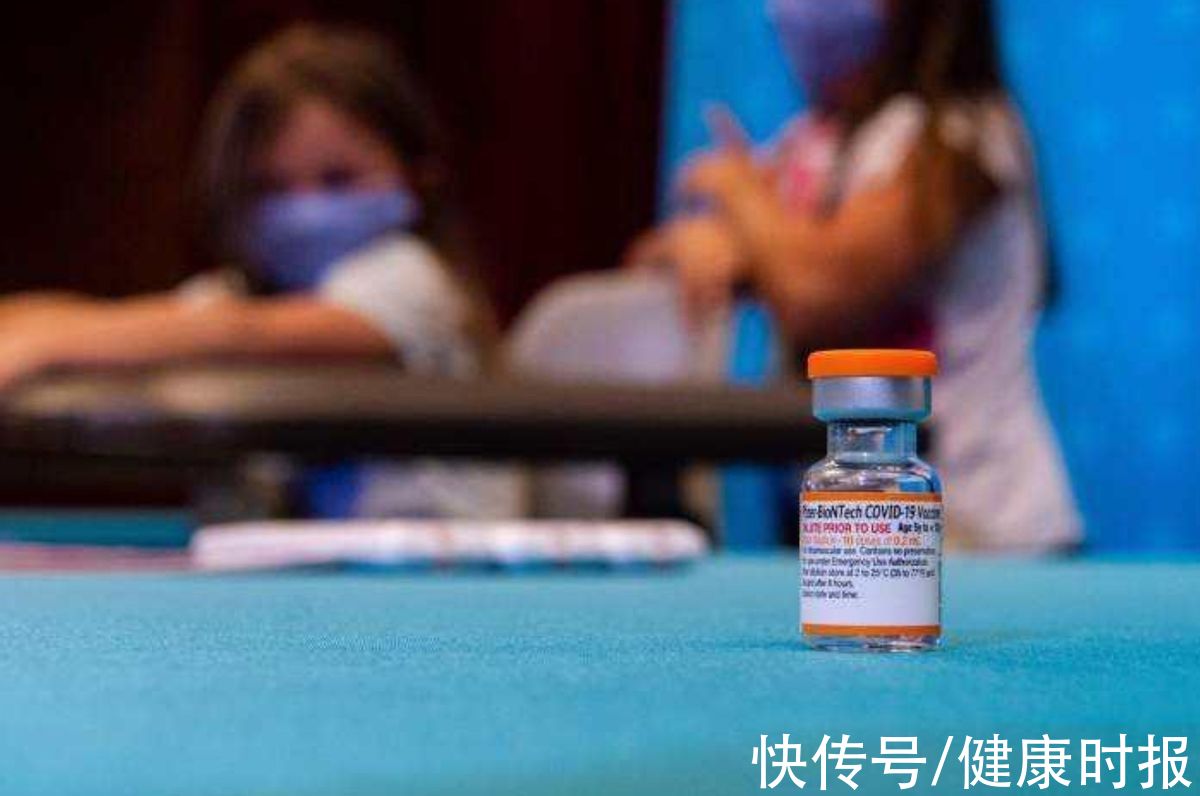
文章插图
图片源自新华社。
【 两款新冠特效药在国内获批,患者何时能用上?】根据美国食品药品监督管理局(FDA)的提示,Paxlovid由奈玛特韦片(nirmatrelvir)和利托那韦片(ritonavir)组成,奈玛特韦片可以抑制SARS-CoV-2蛋白的复制,而利托那韦片可以减缓奈玛特韦片的分解,帮助药物在更高浓度下更长时间地留在体内。治疗时服用三片药,即两片奈玛特韦片和一片利托那韦片,每天口服两次,持续5天,且不能连续使用超过5天。
美国食品药品监督管理局在一份声明中强调,对于那些建议接种新冠病毒疫苗和加强剂量的个人来说,Paxlovid不能替代疫苗接种。
临床试验数显示,与安慰剂相比,在症状出现的三天内(主要终点),接受Paxlovid治疗的成人与COVID-19相关的住院或因任何原因死亡的风险降低了89%。在症状出现后5天内接受治疗的患者(次要终点)中,住院或因任何原因死亡的风险降低了88%,并且在治疗组中没有观察到死亡。
国内首款新冠单克隆中和抗体:正在推进生产供应事宜2021年12月8日,国家药品监督管理局应急批准腾盛华创医药技术(北京)有限公司新冠病毒中和抗体联合治疗药物安巴韦单抗注射液(BRII-196)及罗米司韦单抗注射液(BRII-198)注册申请,批准上述两个药品联合用于治疗轻型和普通型且伴有进展为重型(包括住院或死亡)高风险因素的成人和青少年(12—17岁,体重≥40kg)新型冠状病毒感染(COVID-19)患者。其中,青少年(12—17岁,体重≥40kg)适应症人群为附条件批准。
2月14日,健康时报采访人员从腾盛华创获悉,该公司正积极推进生产及供应工作,以尽早实现药物上市,以惠及新冠患者。
安巴韦单抗和罗米司韦单抗是我国首家获批的自主知识产权新冠病毒中和抗体联合治疗药物,由清华大学、深圳市第三人民医院及腾盛博药生物科技公司合作研发。
- 顾海东|苏州新增8例新冠病毒阳性感染者 病毒溯源为奥密克戎变异株
- 瑞士|诺瓦瓦克斯向瑞士提交新冠疫苗附条件上市申请
- 保肝护肝|它是养肝明目“特效药”,路边很常见,遇到别错过
- 新冠肺炎|苏州7例确诊病例活动轨迹
- 辽宁|蒲江县新冠肺炎疫情最新动态(2022年2月14日)|国内本土确诊+26,在这四地
- 感染者|关于我市7例新冠肺炎确诊病例、1例无症状感染者活动轨迹的情况通报
- 检测|苏州新增7例新冠肺炎确诊病例、1例无症状感染者 活动轨迹公布
- 感染者|苏州公布7例新冠肺炎确诊病例、1例无症状感染者活动轨迹
- 感染者|苏州新增7例新冠肺炎确诊病例、1例无症状感染者 活动轨迹公布
- 感染者|苏州通报7例新冠肺炎确诊病例、1例无症状感染者活动轨迹
