文章图片
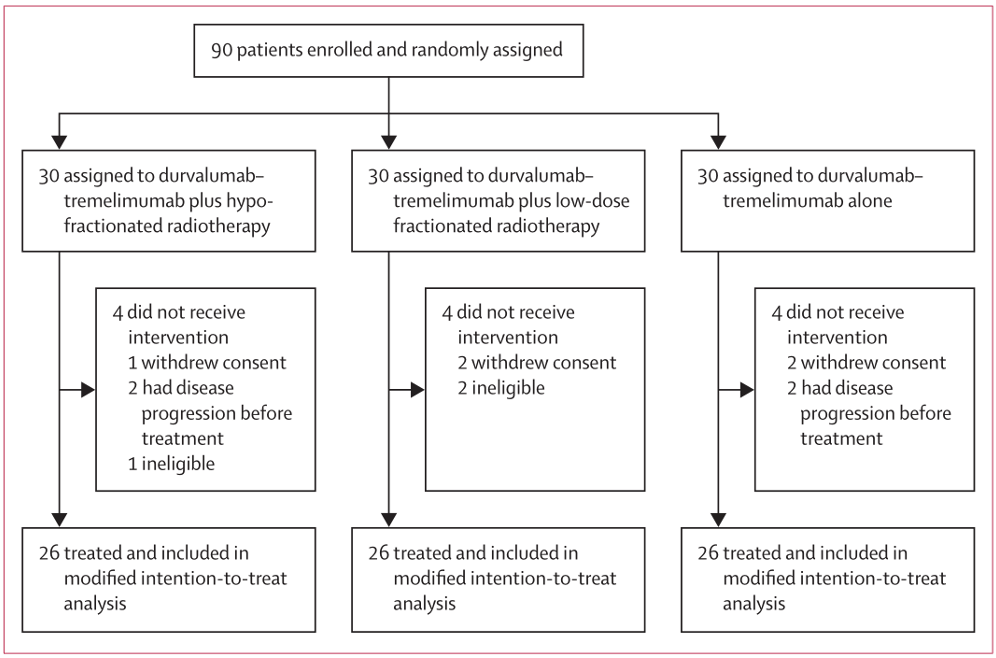
▲ 临床试验开展方案概要
总的来说研究结果令人失望 ,双免疫联合低剂量放疗(7.7% , 0.0-16.3;p=0.64)或大分割放疗组(11.5% , 1.2-21.8;p=0.99)的总体应答率与双免疫组(11.5% , 90% CI 1.2-21.8)之间并无显著差异 。

文章图片
▲ 各组患者接受治疗后的反应率
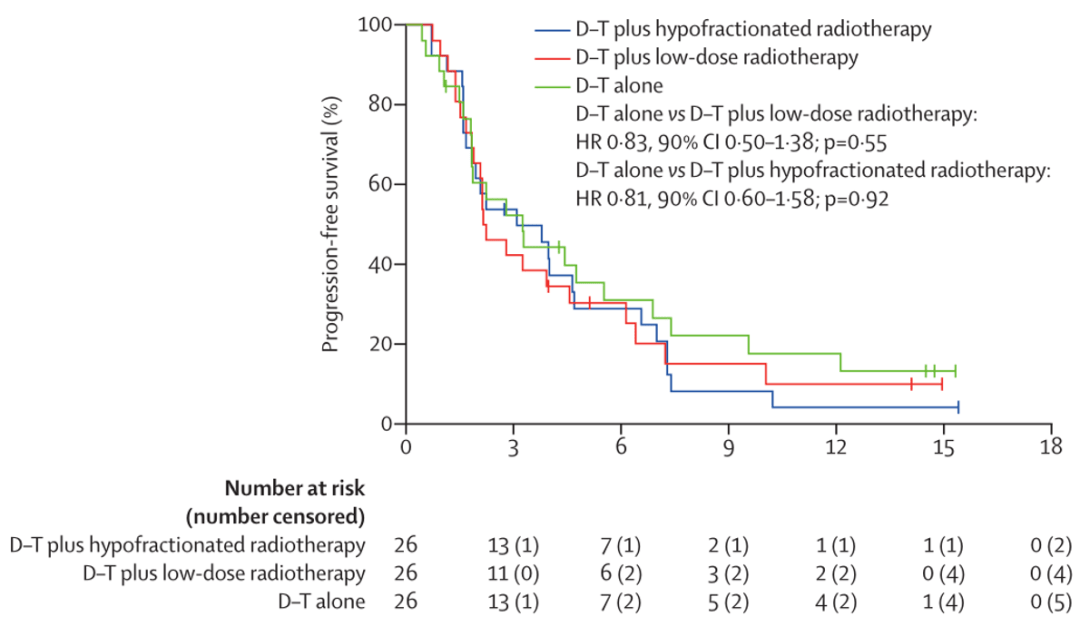
对各组中无进展生存患者(18个月)的比例进行统计 ,发现双免疫组、联合低剂量放疗组与大分割放疗组的比例分别为81%、85%和92% , 但遗憾的是 , 各组无进展生存期之间亦无显著差异(双免疫组的中位数为3.3个月;低剂量放疗组的中位数为4.6个月;大分割放疗组的中位数为4个月) 。
文章图片
▲ 各组患者接受治疗后的无进展生存曲线
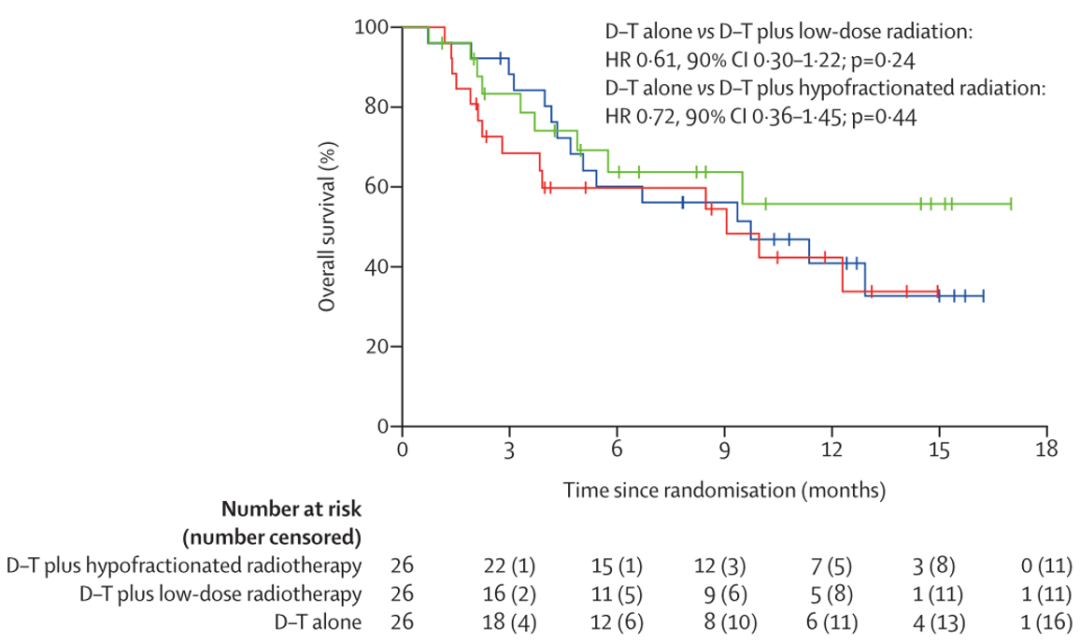
此外 , 总体生存率的结果也不尽如人意 , 各组之间仍然没有显著差异 。
文章图片
▲ 各组患者接受治疗后的生存曲线
Hodi团队对每个治疗周期的治疗相关毒性都进行了评估 , 治疗停止后90天内每30天评估一次 , 并且根据不良事件的通用术语标准4.0版对毒性进行了分级 。
结果显示 , 78例患者中有59例(76%)发生了可能与治疗相关的不良事件 , 最常见的3级或3级以上不良事件分别是呼吸困难 (双免疫组2例 , 低剂量放疗组3例 , 大分割放疗组3例)和低钠血症 (双免疫组1例 , 低剂量放疗组2例 , 大分割放疗组3例) 。
进一步分析发现 , 双免疫组发生了1例(4%)与治疗相关的严重不良事件(黄斑丘疹);低剂量放疗组发生了5例(19%)与治疗相关的严重不良事件 , 包括腹痛、腹泻、呼吸困难、低血钾和呼吸衰竭等;大分割放疗组发生了4例(15%)与治疗相关的严重不良事件 (肾上腺功能不全、结肠炎、腹泻和低钠血症) 。
总的来说 , 这个随机临床2期试验 是迄今为止首个研究CTLA-4抑制剂联合PD-L1抑制剂与放疗联用的前瞻性成果 , 评估了放疗在既往PD-1/PD-L1靶向治疗有进展的NSCLC患者中仅作为系统免疫激活剂的效用 。
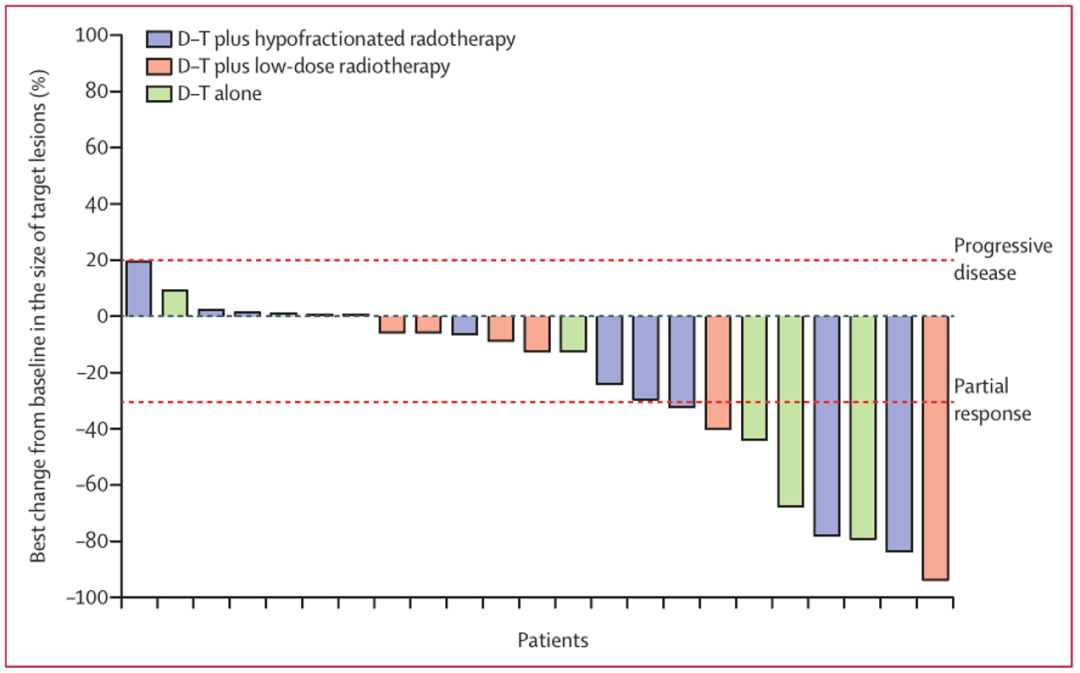
尽管没有取得临床效益上的突破 , 但 研究人员获得了PD-L1抑制剂与CTLA-4抑制剂联合使用治疗PD-1/PD-L1耐药患者的安全性数据 , 并通过中位随访12.4个月 , 发现治疗后发生进展性疾病的患者数量减少 , 同时 , 对治疗发生反应的患者数量增加 。 因此 , Hodi团队确定了PD-L1抑制剂与CTLA-4抑制剂联合使用对表现出应答的部分患者具有重大临床意义 。
文章图片
▲ 疾病控制或有反应患者的病灶区域较基线的变化(n=23)
Hodi和他的同事指出 , 未来的研究应该筛选出预测性的生物标志物(如T细胞浸润) , 以改进治疗方案选择或提高患者反应率和临床效益 。
参考文献:
4.Schoenfeld AJ, Hellmann MD. Acquired Resistance to Immune Checkpoint Inhibitors. Cancer Cell. 2020;37(4):443-455. doi:10.1016/j.ccell.2020.03.017
6.Rizvi NA, Cho BC, Reinmuth N, et al. Durvalumab With or Without Tremelimumab vs Standard Chemotherapy in First-line Treatment of Metastatic Non-Small Cell Lung Cancer: The MYSTIC Phase 3 Randomized Clinical Trial [published correction appears in JAMA Oncol. 2020 Nov 1;6(11):1815]. JAMA Oncol. 2020;6(5):661-674. doi:10.1001/jamaoncol.2020.0237
- 学习用品|事关孩子视力!3月1日起,《儿童青少年学习用品近视防控卫生要求》正式实施
- 香雪制药|香雪制药橘红痰咳液、抗病毒口服液被纳入《中成药防治新型冠状病毒肺炎专家共识》
- 问题|综艺《11点睡吧》:开启健康睡眠新风尚
- 网络|20220310《健康加油站》预告:重视青光眼随访,防止视功能损伤
- 教练|《蝙蝠侠》猫女!戒掉咖啡、不用私人教练,也能养成蚂蚁腰!
- 《自然》子刊:经常喝酒的你,大脑正在慢慢变小
- 新舞|新歌新舞丨玉霞广场舞《靠山不靠山》
-  |公开课丨《你在我心里下了一场雨》炫酷舞姿来袭
- 报告|《当代女性健身洞察报告》发布,女性“请私教”占比为男性2倍
- 本文转自:DV现场《诗经 · 卫风 · 木瓜》:“投我以木瓜|实现吃“瓜”自由,还得是它!
