肺癌目前仍是癌症中致死人数最多的“头号杀手” , 不过近年来免疫治疗的出现 , 显著改善了驱动基因阴性NSCLC患者的治疗效果 , 尤其是达到缓解的患者有望实现长期生存[1] 。
在标志性的临床研究中 , PD-1抑制剂单药治疗PD-L1高表达患者的客观缓解率能够达到40% , 这部分患者大多是能够持久获益的幸运者[2] 。 然而这也同时意味着 , 大部分NSCLC患者对单药免疫治疗并不会产生应答 , 而且哪些特征能够提示患者会对治疗有应答 , 目前也并没有被研究透[3] 。
近日 , 由美国基因泰克(Genentech)公司Romain Banchereau和David S. Shames两位科学家领衔的研究团队在《癌细胞》( Cancer Cell )发表重要研究成果 , 他们发现 肿瘤内浆细胞可以作为NSCLC免疫治疗的预后分子标志物[4] 。
文章图片
论文首页截图
研究团队分析来自两个大规模随机临床试验的891例NSCLC患者转录组数据 , 发现 肿瘤内基线B细胞特征基因表达更多的患者 , 经PD-L1抑制剂单药治疗后总生存期(OS)显著延长 , 死亡风险下降超过30% 。 而且 , 这种关联性与CD8+T细胞无关 , 也不会出现在接受化疗的患者人群中 。
一直以来 , 寻找免疫治疗预后分子标志物都是癌症免疫治疗领域的研究热点 。 在这之前 , 有研究阐述了肿瘤浸润CD8+T细胞在多种癌症类型中与免疫治疗效果的关系[5] 。
最近还有多项研究发现 , 在黑色素瘤、软组织肉瘤以及肾细胞癌的免疫治疗中 , B细胞特征基因高表达的患者有更好的预后 。 但是关于B细胞是否是NSCLC的免疫治疗预后分子标志物的问题 , 仍然没有定论[6,7,8] 。
因此 , 研究团队分析了POPLAR、OAK两项免疫二线单药治疗临床研究的891例NSCLC患者治疗前肿瘤样本转录组(bulk-seq)数据 , 深入探究了上述问题 ,两项研究均使用阿替利珠单抗(PD-L1抑制剂)进行免疫单药治疗 , 对照组均为多西他赛化疗 。
研究者首先将患者按照治疗方案分为两组 , 同时又将同一种治疗方案的患者按照生存期分为两组——小于6个月和大于12个月 , 分析了每种方案内两组患者的差异表达基因 。
在免疫治疗组中一共有817个差异表达基因 , 在长生存期组中过表达的基因富集于B细胞和浆细胞生物学通路中 , 而与效应T细胞相关的基因差异并不显著 。 上述基因表达改变在化疗组中均不显著 , 表明这些B细胞和浆细胞相关基因的预后预测能力只存在于免疫治疗中 。
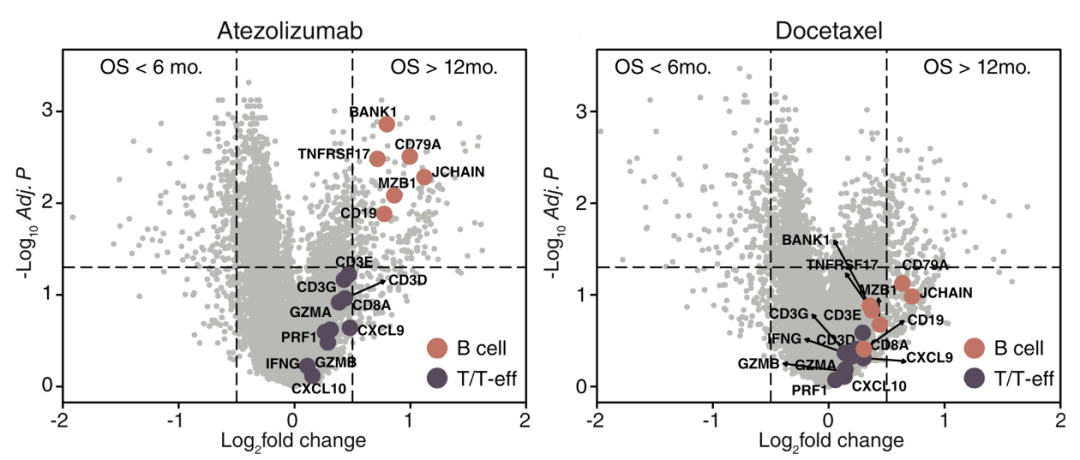
文章图片
B细胞和浆细胞特征基因的高表达与预后更好有关 , 并且这种关系只存在于NSCLC免疫治疗中
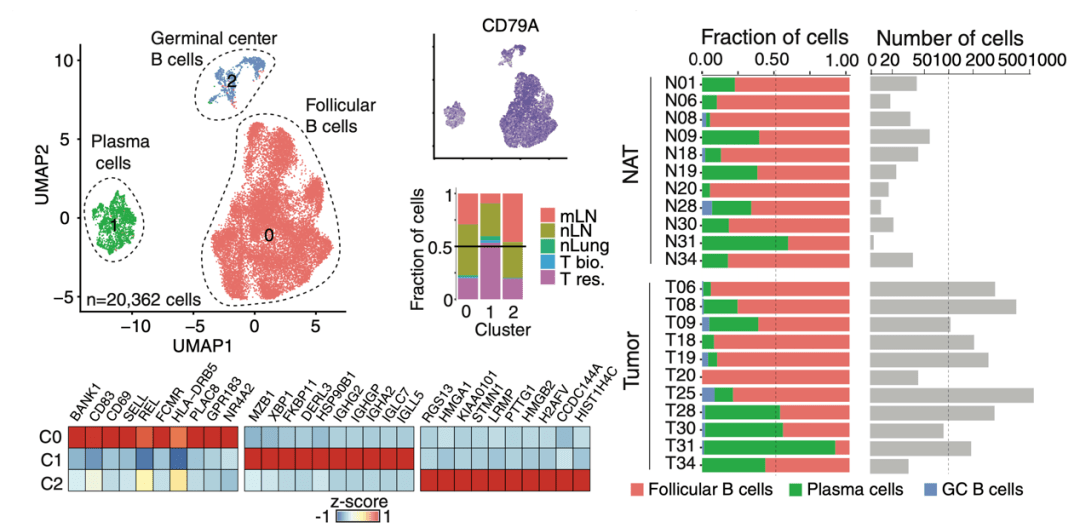
文章图片
在单细胞数据发现了三类CD79A+B细胞亚型 , 并且肿瘤组织中B细胞数量比癌旁组织多
尽管研究人员找到了三种B细胞亚型的特征基因 , 但为了确保这些基因是这三种B细胞亚型的特异基因 , 他们将这些基因在B细胞中的表达量与它们在其他免疫细胞以及基质、上皮、肿瘤细胞中的表达量作了对比 , 最终只选择特异性最高的基因 。
为了证明在单细胞数据中找到的三种B细胞的特异性基因也可以在bulk-seq中准确的代表B细胞 , 研究人员做了进一步的验证 。 他们首先分析了三种B细胞类型的特征基因在bulk-seq(他们自己的数据)的共表达模块 , 发现这些基因有着不错的共表达特性(同一个样本中 , 三种基因同时表达或不表达) , 初步表明这些基因能在bulk-seq代表三种B细胞 , 并且有着较好的一致性 。
- 细胞|JITC:颠覆认知!科学家首次发现PD-1抑制剂竟保护特定肠癌细胞,促进结直肠癌生存,免遭放化疗杀伤丨科学大发现
- 中药|《药典》点名:3种中药被禁用,不仅伤肝还致癌,别以为是好药
- 《春季锻炼指南》为您推荐那些春天适宜的运动
- 本文转自:CCTV热线12最近几年|遏制“食金之风”:金箔毫无营养价值,价格虚高潜藏隐患丨《热线12》
- 治疗|由肾病发展到肾衰竭,或会有四种特征,早了解早预防
- 本文转自:全民健康生活方式行动“迟日江山丽|《春季锻炼指南》为您推荐那些春天适宜的运动~
- 强度|《春季锻炼指南》为您推荐那些春天适宜的运动
- 灵芝的5大养生功效
- 起床气|长寿的人有共性?汇总6个特征,照着做,你也可以长寿
- 黑眼圈|肾不好的人,都写在脸上!脸上几个特征明显,劝你排查肾病
