
文章图片
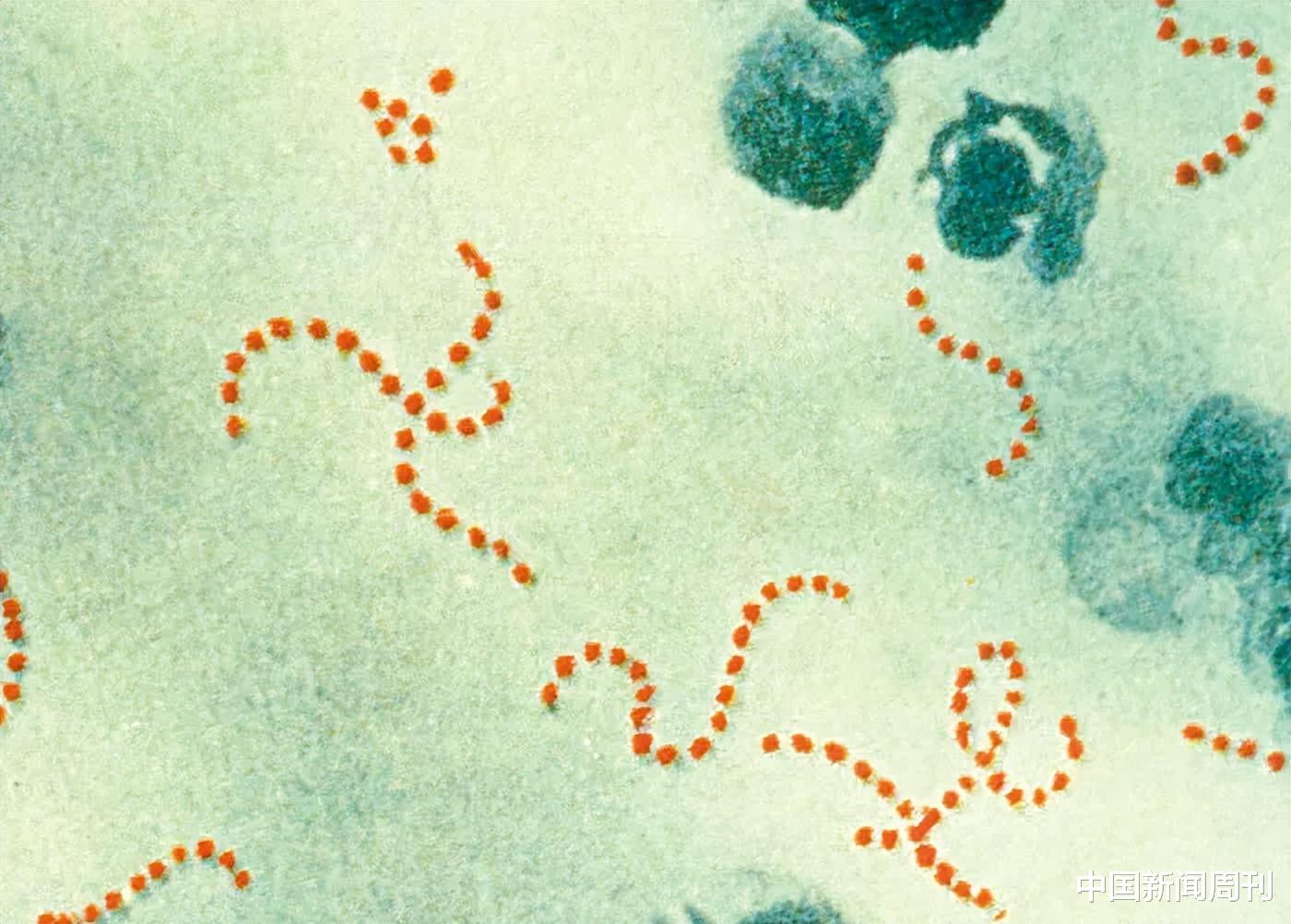
“食人菌”感染眼下在日本似乎愈演愈烈 。
6月18日 , 日本国立感染症研究所公布的数据称 , 截至6月9日 , 日本今年报告的链球菌急性中毒休克综合征(STSS) , 即俗称的“食人菌”感染症 , 病例数累计破千 , 达1019例 。 日本的“食人菌”感染病例在今年上半年已超过去年全年病例数 , 由此引发日本国内关注和恐慌 , 也让周边国家相当紧张 。
“食人菌”的危险性到底有多大?它能否导致大范围感染?我们该如何防护?
(资料图片)东京街头的人群 。 图/视觉中国
有症状到脏器衰竭
只需24至48小时
“食人菌”感染只是一种夸张的说法 。 日本的一些患者死亡是因β-溶血性链球菌感染导致的STSS 。 STSS的致死率超过30% 。
β-溶血性链球菌的全称是A族β-溶血性链球菌 。 1874年 , 奥地利外科医生西奥多·比尔罗特在治疗丹毒和伤口感染病人时首次发现 , 病人的血液中有一种链球状微生物 , 认为这是引发感染的病原体 。 1879年 , 法国微生物学家路易斯·巴斯德首次分离出链球菌 。
1932年 , 英国医生安德鲁斯和克里斯蒂把不同医生和研究人员观察到的链状球菌命名为化脓性链球菌 。 大多化脓性链球菌能产生外毒素使人致病 。 溶血性是链球菌的一个特征 , 化脓性链球菌通常为β-溶血 , 具有完全溶血性 。 1933年 , 美国微生物学家瑞贝卡·兰斯菲尔德创建了兰斯菲尔德链球菌分类法 , 将链球菌分为18—20个族(组或群) , 其中对人体致病的链球菌以A族为主 。
溶血性链球菌可引起非侵袭性、侵袭性疾病 , 以及感染后免疫并发症 , 非侵袭性疾病包括咽炎、猩红热、坏死性筋膜炎等 , 侵袭性疾病包括STSS、脑膜炎等 。
STSS并不是一种新型感染症 。 根据文献记录 , 美国1987年报告了首例病例 , 之后 , 欧洲、亚洲也报告了病例 。 日本也在1992年报告了最早的典型病例 , 此后每年确诊病例为100—200例 。
本质上 , STSS是一种由溶血性链球菌引发的败血性休克 , 特点是发病急 , 初期一般是咽喉疼痛、发烧以及食欲不振、腹泻、呕吐等 , 还有低血压等症状 , 继而可出现软组织病变、呼吸衰竭、肝功能衰竭、肾功能衰竭等多脏器衰竭 。 患者从出现症状到发展为休克和多脏器衰竭只需24至48小时 。
A族β-溶血性链球菌引起的其他侵袭性疾病也不少见 。 美国每年A族β-溶血性链球菌引起的侵袭性疾病患者超过1.5万例 , 约有1600人死亡 , 加拿大这类疾病的患病率为每年5.24/10万人 , 英国则是每年2.9/10万人 。 不过 , STSS引起的死亡率在该种细菌引发的疾病中最高 。
电子显微镜下的化脓性链球菌 。 图/视觉中国
过去 , 溶血性链球菌主要感染儿童 , 常引起5—9岁年龄段儿童患猩红热 。 此外 , 每年冬春季时 , 儿童中会流行链球菌性咽炎 , 以及在夏秋季 , 儿童易感染链球菌性脓疱病 。 溶血性链球菌引起人感染的原因是 , 它们可以寄生在人体咽部和不洁皮肤表面 , 引起浅表性感染、侵袭性感染、毒素介导性疾病等 。
溶血性链球菌的主要宿主是人类 , 主要通过空气飞沫、皮肤黏膜接触传播 。 因此 , 卫生条件差、居住拥挤情况 , 有利于溶血性链球菌的传播 。 溶血性链球菌感染的另一个途径是 , 通过污染的食物传播 。 溶血性链球菌易感染5—15岁儿童、老年人及免疫力低下者 。
最近几年 , 世界卫生组织的评估表明 , 现在全球约1800万人感染溶血性链球菌 , 而且每年新增1.1亿溶血性链球菌脓疱疮、6.1亿溶血性链球菌急性咽/扁桃体炎、178万溶血性链球菌严重感染病例和51.7万死亡病例 。
或与链球菌变异有关
日本的“食人菌”感染症多发于30岁以上的成年人 , 而且 , 今年以来50岁以上感染者增多 , 尤其70岁以上的感染者人数比往年出现了大幅上升 。
一般情况而言 , 创造良好的卫生条件是减少溶血性链球菌感染的关键 。 目前 , 世界上发达国家溶血性链球菌发病率已显著下降 。 日本是卫生条件比较好的发达国家 , 为何还出现大量“食人菌”感染?
根据日本国立感染症研究所6月18日发布的数据 , 6月3日—9日这一周 , 日本全国约3000家定点医疗机构平均每家机构报告A族β-溶血性链球菌性咽炎4.87例 , 是2023年同期的约3倍 。
对于STSS为何在日本激增 , 目前还难以给出科学的证据和解释 , 有推测称 , 与新冠疫情解除隔离后人们的生活方式有关 。 传染病专家、东京大学医学院教授菊池健表示 , 因为很多人没有遵守新冠大流行期间的手部消毒等基本感染预防措施 。 不过 , 这难以解释为何只是STSS增多 , 其他感染性疾病没有同时增多 。
一个可能稍具说服力的原因是 , 溶血性链球菌发生了基因突变 , 导致毒力增加 。 英国等欧洲国家从2014年开始 , 儿童猩红热开始增加 。 从1999年到2013年 , 英国猩红热的发病率由3.1/10万增长至8.2/10万 , 2014年发病率升至27.2/10万 。 到了2022年 , 法国、爱尔兰、荷兰、瑞典都观察到猩红热病例有所增加 , 主要影响10岁以下儿童 。
在对猩红热患者的病原体分离和研究后发现 , 一种新的M1UK谱系菌株是导致发病人数增多的重要原因 , 它有27个基因发生突变 , 这种菌株会产生较多毒素 , 而且容易传播 。
之后 , 欧洲和亚洲一些国家也发现了M1UK型A族β-溶血性链球菌 , 结果不只导致这些国家猩红热发病人数增加和病情严重 , 就连其他A族β-溶血性链球菌侵袭性疾病的发病人数也在增多 , 其中 , 就包括STSS 。
现在 , 日本STSS患者增多 , 死亡人数也增加 , 可能与M1UK谱系菌株基因突变后的毒力增加有关 。 但是 , 这也需要研究进一步证实 。 也有一些专业人员推测 , 患者对于链球菌刺激产生了过度免疫反应 , 人体免疫系统释放了过多细胞因子 , 最终导致休克和多器官功能衰竭而死亡 。
不太可能大范围传播
中国每年也会有A族β-溶血性链球菌引起的侵袭性疾病 , 其中也会有STSS , 但是大多是零星病例 , 且主要是儿童感染 。 目前 , 中国还没有发现成人感染“食人菌”的病例 。 国内一项研究收集了2003年—2021年间50例STSS病例 , 患者都是儿童和青少年 , 年龄范围为出生5小时至17岁 , 以3岁以下婴幼儿为主 , 最终治愈10例 , 好转10例 , 死亡28例 。 而且 , 经过使用含青霉素的抗菌方案可提高儿童STSS的治疗效果 。
这些情况说明 , 过去和现在中国尽管也有“食人菌”感染 , 但是病例较少 , 且主要是儿童 。
虽然类似日本的“食人菌”感染症还没有在中国出现 , 但也需要防范 。 国内年龄大的人群需防范“食人菌”感染症 。 日本“食人菌”感染症的一个特别症状是疼痛 , 多发生于四肢 。 如果出现手脚疼痛和肿胀 , 有比较强烈的咽喉疼痛等 , 需及时就医 。 同时 , 在日常生活中 , 勤洗手、戴口罩等防护措施对预防感染也有效 。
对A族β-溶血性链球菌感染 , 现在的抗生素治疗是有效的 , 青霉素、阿莫西林、头孢类抗生素的疗效都较好 , 但是 , 治疗需在医生的指导下进行 , 不要过早停药 。 当然 , STSS要综合治疗 , 使用抗生素的同时 , 要根据具体情况纠正酸中毒、改善微循环等 。 只要及早诊治 , 链球菌感染不太可能大范围传播 。
发于2024.7.1总第1146期《中国新闻周刊》杂志
杂志标题:“食人菌”致使日本上千人感染
【致死率超30%!“食人菌”到底是什么?】作者:张田勘
- 姜萍事件又持续升级!30万粉女主持人曝猛料:有人付费请她抹黑姜萍
- 金哲堂表示:从零起步!30天锻炼计划,健身小白也能变达人
- 一日三餐减肥食谱示例,坚持30天,让你暴瘦一圈
- 这种饮料喝着不甜,但升糖能力超高!很多人不知道还天天喝
- 刚开始跑步,心率必须小于130吗?控制不住怎么办?
- 不想累死累活?试试低心率跑步,效果超乎想象!
- 一天做对 9 件燃脂小事,30天暴瘦15斤
- 雌激素不足?6种超级食物激活雌激素,每天换着吃,保持年轻态
- 每天做30个深蹲,身体迟早会收获3大好处,但提醒大家:需坚持!
- 运动超过30分钟才会消耗脂肪吗?这篇文章告诉你答案
