血栓|阿斯利康新冠疫苗诱发血栓机制如何?加拿大团队《自然》刊文
新冠疫苗的安全性仍是重中之重 , 其中牛津-阿斯利康新冠疫苗ChAdOx1产生的相关血小板减少症和血管等不良事件导致一些国家限制其使用 。 北京时间7月7日傍晚 , 顶级学术期刊《自然》(Nature)以“加快评审文章”(Accelerated Article Preview)形式在线发表了由加拿大麦克马斯特大学、麦克马斯特输血研究中心等团队联合完成的一项研究 , 题为“Antibody epitopes in vaccine-induced immune thrombotic thrombocytopenia” 。

文章图片
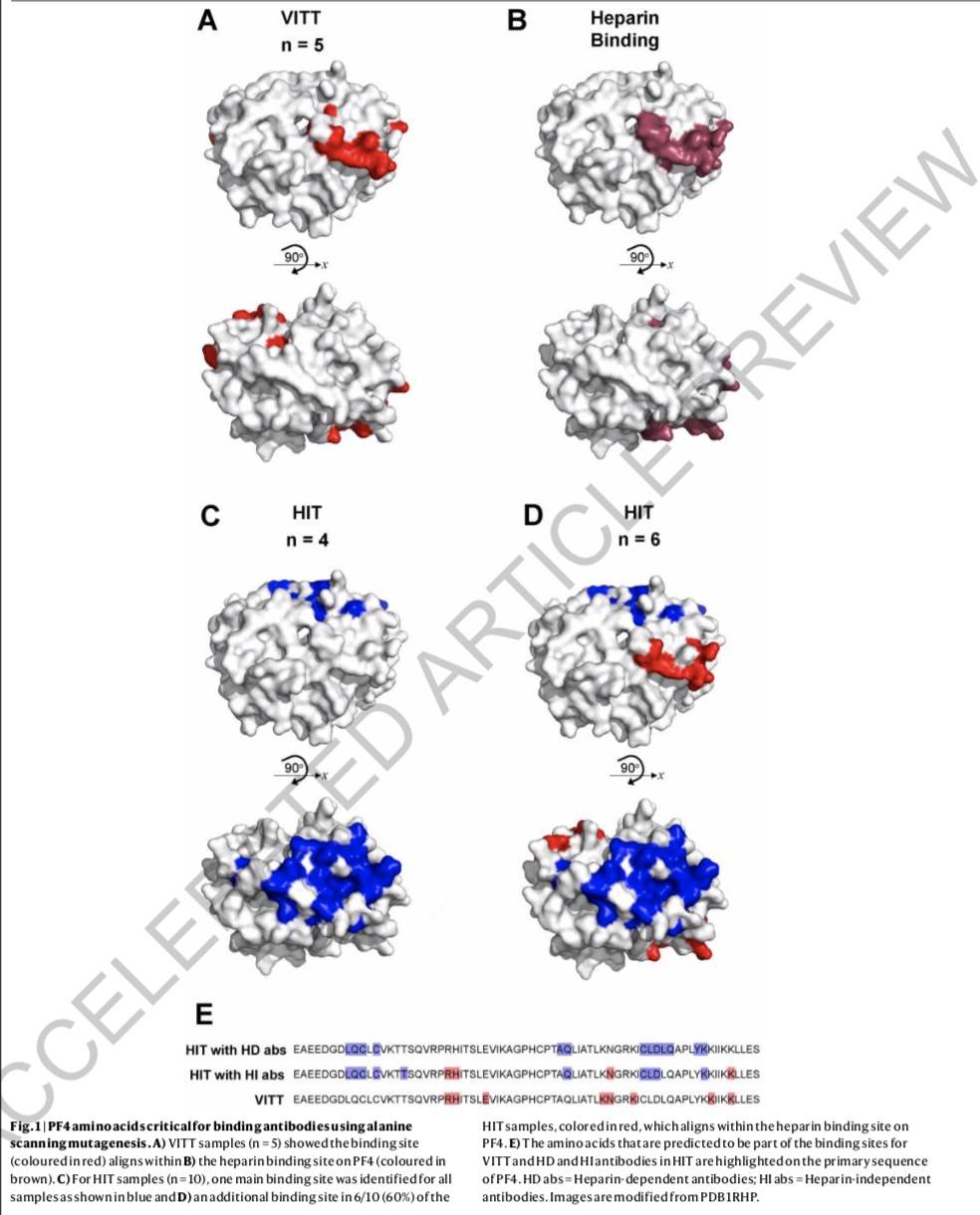
该研究阐释了部分新冠疫苗诱导的抗体可能会如何导致“疫苗诱导免疫血栓性血小板减少症”(VITT)这一罕见症状 。 研究发现 , 接种过阿斯利康新冠疫苗(ChAdOx1)的5位VITT患者的抗体会与一个参与凝血的蛋白结合 , 且结合位点和抗凝血药物肝素与该蛋白结合的位点相同 。
论文写道 , VITT是在接种腺病毒载体新冠疫苗后出现的一种罕见但严重的不良反应 , 其临床表现为中度至重度血小板减少以及动脉或静脉出现血液凝块 。 值得注意的是 , VITT被认为有点像“肝素诱导血小板减少症”(HIT) 。 据推测 , VITT与HIT具有相似的病理生理机制 , 一些研究人员已经证明VITT和HIT一样 , 检测样本中存在高水平的抗PF4抗体 。 PF4是一种能与血小板结合的蛋白 , 会参与凝血 。
但是 , 这些抗体导致VITT的具体机制一直不太清楚 。 论文中写道 , VITT是一种独特的综合征 , 因为它在没有肝素暴露的情况下发生 , 而且体外血小板反应模式不显示典型的肝素依赖 。
文章图片
【血栓|阿斯利康新冠疫苗诱发血栓机制如何?加拿大团队《自然》刊文】在这项最新的研究中 , 研究人员分析了接种过一剂阿斯利康疫苗的5位VITT患者的血清 , 他们的平均年龄44岁(范围35-72岁)、女性占比40% 。 从首次接种阿斯利康疫苗到采集样本的时间为14-40天(平均28天) 。
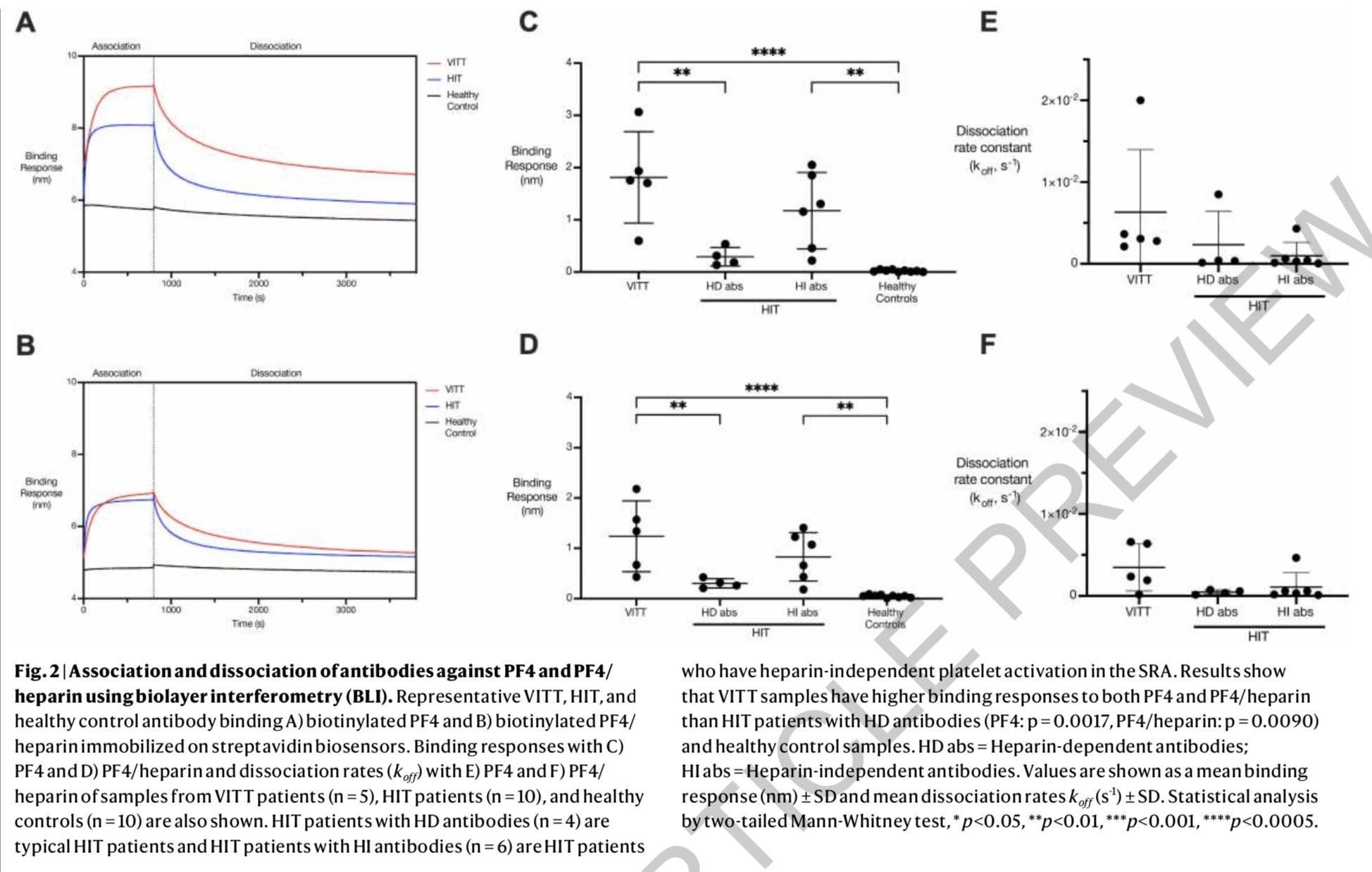
研究发现 , 从这些患者血清中获得的抗体与PF4结合的位点和肝素相同 。 将其与10位HIT患者的血清样本进行比较后 , 研究人员发现VITT抗体与PF4的结合反应更强烈 。
研究人员认为 , VITT抗体与PF4结合后会形成免疫复合物 , 这些复合物随后通过血小板表面的FcγRIIa受体激活血小板 , 这或许会引起凝血 , 导致血小板减少症和血栓形成 。
但他们同时也指出 , 这或许不是导致VITT患者出现血栓形成事件的唯一因素 , 其他血清因子可能也参与了血小板活化 。
文章图片
实际上 , 除上述研究外 , 也有其他实验团队在关注阿斯利康新冠疫苗 。 此前的北京时间6月9日晚间23时 , 国际顶级学术期刊《自然-医学》(Nature Medicine)也在线发表了由英国团队完成的一项研究 , 题为“First-dose ChAdOx1 and BNT162b2 COVID-19 vaccines and thrombocytopenic, thromboembolic and hemorrhagic events in Scotland” 。 该研究对超过250万名接种过第一剂牛津-阿斯利康新冠疫苗ChAdOx1或辉瑞-BioNTech新冠疫苗BNT162b2的苏格兰成年人进行了全国性调查 。
调查表明 , 阿斯利康疫苗和一种自体免疫出血性疾病 , 即免疫性血小板减少性紫癜(immune thrombocytopenic purpura , ITP)的风险轻微升高有关 。 研究还发现 , 可能有证据表明 , 阿斯利康疫苗与其他出血及血管问题风险升高有关 。 据估计 , 每十万例第一剂注射中发生1.13例 。
这支英国团队当时强调 , 公共卫生当局应将这些与阿斯利康疫苗相关的相对较小的风险升高告知其辖区 。 “如果新冠疫苗供应充足 , 为公众提供其他的替代疫苗可能是必要的 。 ”
- 身体|脑血栓发病前,身体或发出4个“警示”,需留心观察,别错过了
- 甘油三酯超过1.7,别急着用药,做好3件事,或能避免血栓“光临”
- 体内有血栓身体会发出这些信号,做好这三点,让血管更通畅
- 荞麦|是一种天然的“清栓王”,如果你经常吃,血栓可能会悄悄地远离你
- 血栓|眼睛有三个信号,是血脂已高,防血栓,做好“戒三物,远四习”!
- 心脑血管疾病|血栓天敌被发现了,每天吃2口,清血管冲走血栓,杜绝高血脂
- 血栓|血液“稀释剂”已公布,不是枸杞,常吃疏通血管,头晕眼花自动消
- 血栓|体内有血栓,心梗、脑梗跟着来!预防血栓形成,3个办法教会你
- 血液|6味中药,传承了500年,开水一烫,血液不再粘稠,血脂血栓全溶光
- 静脉|【护理科普】带您了解抗血栓梯度压力袜
