敲除肿瘤细胞上的PD-L1对疗效没有明显影响 , 但敲除树突状细胞上的PD-L1后 , 双抗的治疗效果消失
这一发现着实让人有些意外 , 如果是直接靶向肿瘤细胞 , 那比较好理解——肿瘤细胞可以直接被T细胞干掉 。 那为何实际上是树突状细胞在这一过程中发挥了更为重要的作用呢?
研究人员首先分析了PD-L1×CD3双抗对肿瘤微环境的影响 。 他们发现 , 在 双抗治疗后 , CD8+ T细胞被更好地激活 , 且增殖能力增强 。 更重要的是 , PD-L1×CD3双抗治疗后 , 肿瘤中抗原特异性CD8+ T细胞的百分比也增加了 。
此外 ,肿瘤微环境的中的免疫抑制型细胞的比例显著降低 。 说明PD-L1×CD3双抗可以重塑肿瘤微环境 , 从而增强特异性抗肿瘤免疫反应 。
那背后的机制究竟是什么呢?
我们都知道 , T细胞的增殖与活化需要树突状细胞等抗原递呈细胞上的B7-1/2(CD80/CD86)与T细胞表面的共刺激受体CD28结合 。 而且此前的研究也表明 , 抗PD-1治疗的疗效依赖于CD28 , 提示共刺激信号在生成和维持T细胞免疫反应中有重要作用(4, 5) 。 因此 , 作者猜测 PD-L1×CD3双抗的治疗效果可能依赖于T细胞的共刺激信号 。
文章图片
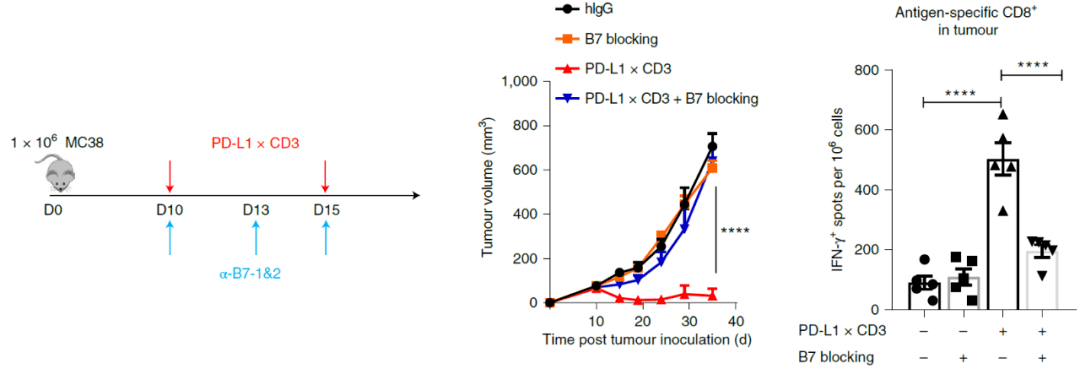
阻断B7-CD28共刺激信号可消除PD-L1×CD3双抗的治疗效果
为了验证这一假设 , 研究人员在使用PD-L1×CD3治疗的同时 , 给予抗CD80/86抗体来阻断B7-CD28共刺激信号 。 结果发现 , 阻断共刺激信号完全消除了PD-L1×CD3的治疗效果 , 提示 PD-L1×CD3治疗通过增强CD28共刺激信号来促进T细胞的活化 , 从而产生有效的抗肿瘤免疫反应 。
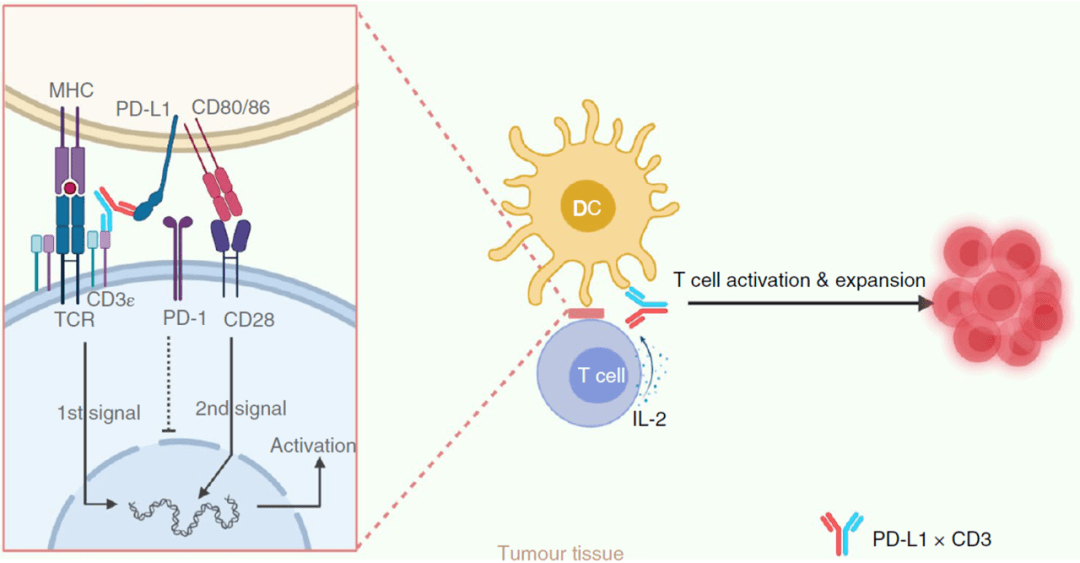
经过这一系列抽丝剥茧般的分析 , PD-L1×CD3抗肿瘤的作用机制终于清晰了:在肿瘤微环境中 , PD-L1×CD3双抗主要通过连接树突状细胞和T细胞来发挥作用 , 这不仅可以通过CD3给予T细胞活化的第一信号 , 还可以阻断PD-1/PD-L1介导的抑制作用 。 同时 , 树突状细胞上的CD80/CD86会与T细胞上的CD28结合 , 为T细胞激活提供第二信号 。 因此 , 肿瘤组织中的T细胞将被重新激活 , 从而产生有效的抗肿瘤免疫反应 。
文章图片
机制总结图
总的来说 , 这项研究 突破了传统的BiTE设计思路 , 将T细胞和树突状细胞连接起来 , 为新一代双特异性抗体的开发提供了新的方向 。 本文的作者也正在开发PD-L1×CD3双抗的改进版本 , 以期进一步增强疗效并降低毒性 。

文章图片
参考文献
1.M. E. Goebeler, R. C. Bargou, T cell-engaging therapies - BiTEs and beyond. Nat Rev Clin Oncol 17, 418-434 (2020).
2.J. Li et al., CD3 bispecific antibody-induced cytokine release is dispensable for cytotoxic T cell activity. Science Translational Medicine 11, (2019).
3.L. Liu et al., Rejuvenation of tumour-specific T cells through bispecific antibodies targeting PD-L1 on dendritic cells. Nat Biomed Eng 5, 1261-1273 (2021).
4.E. Hui et al., T cell costimulatory receptor CD28 is a primary target for PD-1-mediated inhibition. Science 355, 1428-1433 (2017).
【治疗|《自然》子刊:千里姻缘“双抗”牵,DC细胞让T细胞“嗨翻天”!】5.A. O. Kamphorst et al., Rescue of exhausted CD8 T cells by PD-1-targeted therapies is CD28-dependent. Science 355, 1423-1427 (2017).
- 隔离|如何帮治疗、隔离中的孩子做好心理调适?专家给出建议
- 卫生室|《乡村医生诊疗口袋书(先行本)》面世
- 治疗|糖尿病服药后,出现的低血糖比较严重怎么办?
- 相关|【中国实用外科杂志】肥胖代谢病合并甲状腺癌外科治疗中国专家共识(2021版)
- 治疗|治疗运动神经元的方法有哪些呢?
- 国人历来重视精神对治疗疾病、养生保健的重要作用|心平气和,有益健康的“良药”
- 解读|《浙江省医院门诊管理办法》政策解读
- 廉东波|《健谈》观点丨浅表性胃炎三五年复查一次 萎缩性胃炎一年一查
- 治疗|善德医疗·好安森|这6种血糖测量方法,好多人都不清楚!
- 歧视|乙肝容易传染?中医帮你疏肝解郁,软坚散结,治疗乙肝一步到位!
