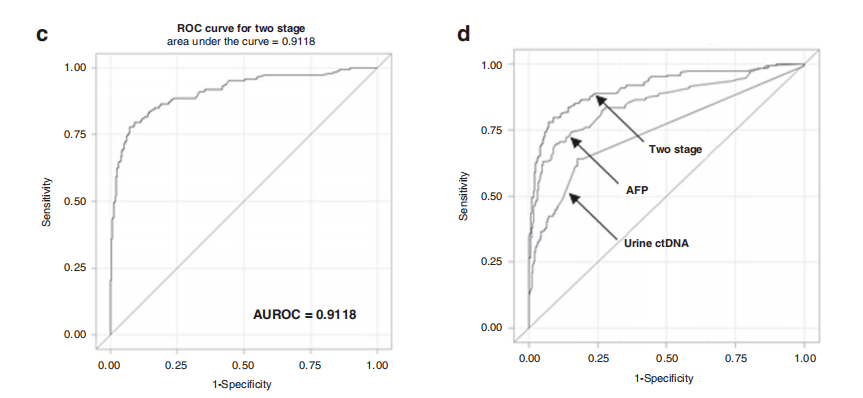
为了更好的从低AFP人群中鉴别HCC患者 , 研究人员提出 以AFP≥20 ng/mL为临界值鉴别HCC的两阶段模型 , 然后在低AFP的亚群上建立AFP和ctDNA联合的logistic模型 。 结果显示: 两阶段模型AUROC为0.9118 , 显著高于仅使用AFP的模型;该模型在特异性为90%时 , 可以从低AFP人群中额外鉴别出60例(60%)HCC患者 。
文章图片
两阶段模型的ROC及相互比较
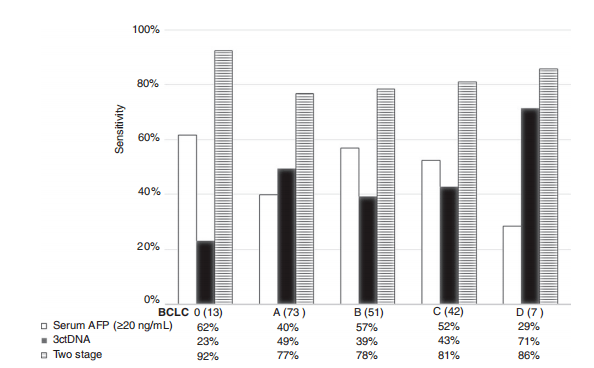
接下来 , 研究人员按肿瘤分期(BCLC分期) , 进一步分析了AFP、尿液ctDNA和两阶段模型在肿瘤不同分期中的总体表现性能 。
结果显示:以AFP≥20 ng/mL为临界值 , 仅使用AFP对BCLC分期0、A、B、C和D期患者检测的敏感性分别为62%、40%、57%、52%和29%;当尿液ctDNA检测特异性为90%时 , 结果分别为23%、49%、39%、43%和71%; 而两阶段模型的敏感性显著提高 , 分别为92%、77%、78%、81%和86% 。
文章图片
三种模型在不同HCC患者分期下的敏感性
由于早期检测是筛查试验的关键 , 研究人员进一步将注意力集中在BCLC 0和A期HCC上 。 分析表明 , 虽然尿液ctDNA检测对BCLC 0期的筛查敏感性较低 , 但所有样本的AFP均<20 ng/mL , 因此 两阶段模型可将敏感性提高到92%;同样 , 在BCLC A期中 , 两阶段模型敏感性从40%提高到77% 。
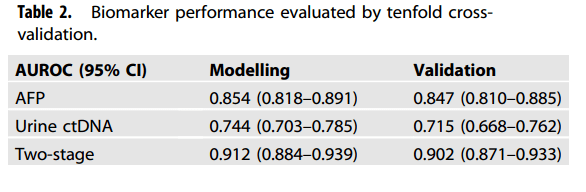
最后 , 研究人员利用十倍交叉验证来检验模型预测的稳健性 。 结果表明 , 两阶段模型是稳健的 , 其AUROC从训练集0.912降至验证集0.902 , 且在90%特异性下 , 其敏感性仅损失1% , 从79.6%降至78.6% , 无显著差异 。
文章图片
十倍交叉验证评估检测模型性能
值得注意的是 , 两阶段模型在应用于临床HCC筛查之前 , 还需要盲法验证做进一步的评估 。 另外 , 本研究为横断面研究 , 没有连续性收集样本或额外采集影像数据 , 这些协变量可能对未来ctDNA的应用提供有价值的信息 , 有可能应用到病变太小 , 无法通过标准筛查法检测的癌前病变或肝癌患者 。
HCC的早期筛查和诊断对患者的预后至关重要 , 尿液ctDNA检测作为HCC筛查的一种新的非侵入性检测方法 , 尤其是在低AFP和早期肝病患者中表现出良好的筛查性能 , 具有潜在的临床应用价值 。

文章图片
参考文献:
[1] Heimbach JK, Kulik LM, Finn RS, et al. AASLD guidelines for the treatment of hepatocellular carcinoma. Hepatology. 2018;67(1):358-380. doi:10.1002/hep.29086
[2] Ferlay J, Soerjomataram I, Dikshit R, et al. Cancer incidence and mortality worldwide: sources, methods and major patterns in GLOBOCAN 2012. Int J Cancer. 2015;136(5):E359-E386. doi:10.1002/ijc.29210
[3] Yang JD, Dai J, Singal AG, et al. Improved Performance of Serum Alpha-Fetoprotein for Hepatocellular Carcinoma Diagnosis in HCV Cirrhosis with Normal Alanine Transaminase. Cancer Epidemiol Biomarkers Prev. 2017;26(7):1085-1092. doi:10.1158/1055-9965.EPI-16-0747
[7] European Association for the Study of the Liver. Electronic address: easloffice@easloffice.eu; European Association for the Study of the Liver. EASL Clinical Practice Guidelines: Management of hepatocellular carcinoma [published correction appears in J Hepatol. 2019 Apr;70(4):817]. J Hepatol. 2018;69(1):182-236. doi:10.1016/j.jhep.2018.03.019
- 睡眠|“肝癌大户”被揪出!紧急通知:吃1口堪比10斤猪油,趁早撤下桌
- 营养物质|病从嘴入!提醒:2类食物比烟酒还毒,极易引起“肝癌”
- 脂肪肝|牛肉是肝癌的“发物”?内科医生:若养好肝,建议少吃这3种食物
- 时间|养肝的重点是远离3物,若能不碰,肝癌可能会和你无缘
- 肝癌|多位专家联合声明:身体若有亮起3个“红灯”,可能肝癌在“招手”,趁早检查肝
- 陆骊工|肝癌患者生存期可望延长
- 朱震宇|直播预告丨体检这些指标异常就离肝癌不远了?早期肝癌能治好吗?
- 脂肪肝|为何肝癌越来越多?医生:10种食物需少碰,肝或变健康
- 免疫|30岁男子“内卷”4年,确诊肝癌2月离世,医生直言:肝脏受不了
- 肝癌|你知道吗?人体缺乏硒元素诱发多种癌变,它含硒量最丰富,要多吃
