美国|丁肝在研创新药Lonafarnib,口服抑制剂,完成3期D-LIVR注册
丁肝病毒感染也是全球严重的病毒性肝炎之一 , 最近 , 吉利德科学积极推进管道中丁肝新药Hepcludex? (Bulevirtide)在美国本土上市, 已向FDA提交生物制剂许可申请(BLA) 。 与此同时 , 专注于严重罕见病靶向疗法开发公司Eiger BioPharmaceuticals也正推进管道中的口服丁肝抑制剂Lonafarnib , 完成一项3期临床研究D-LIVR的注册工作 , 已有超过400名受试者参加研究 , 预计2022年底发布顶线数据 。
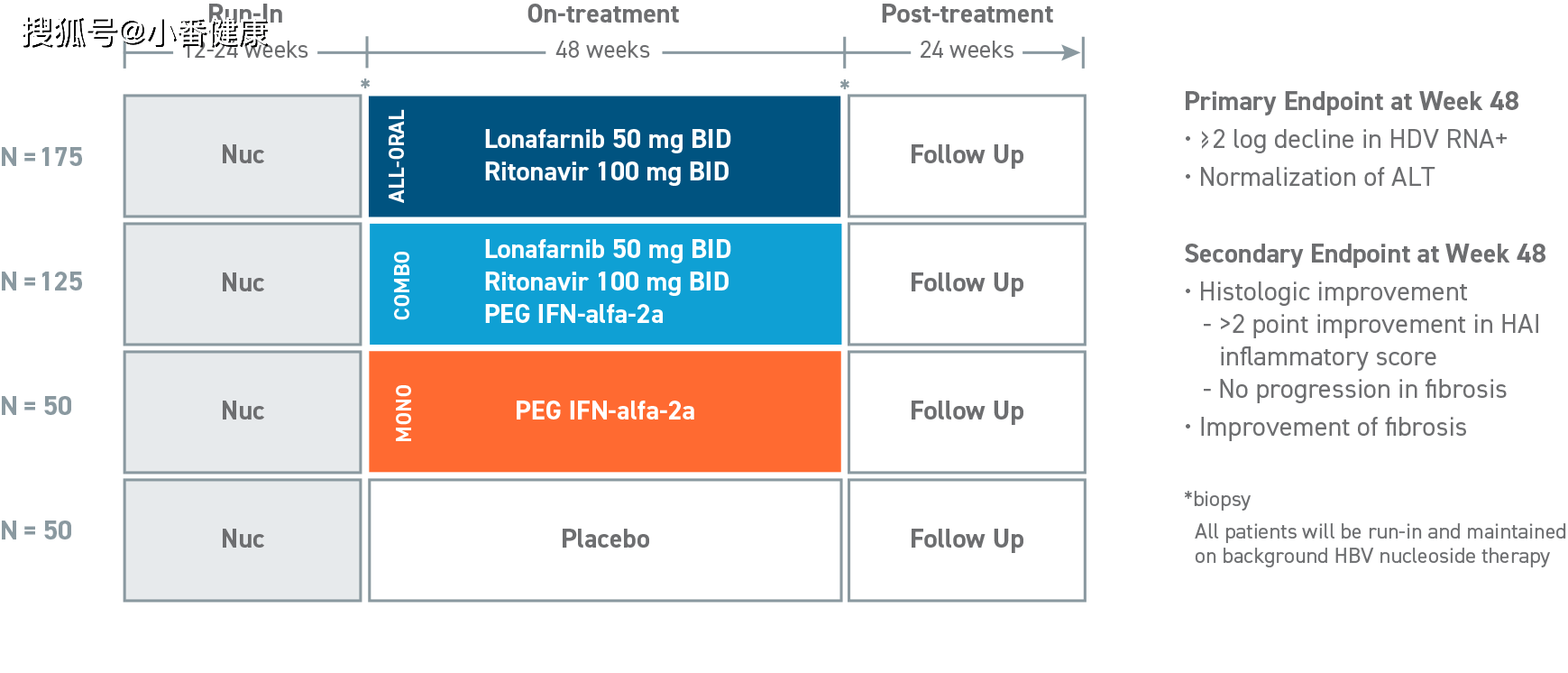
来自:Eiger公司 , D-LIVR:3期全球研究
文章图片
丁肝在研创新药Lonafarnib , 口服抑制剂 , 完成3期D-LIVR注册
一、D-LIVR研究
根据Eiger公司介绍 , D-LIVR(丁肝病毒改善和病毒学反应)是一项全球性、多中心最大规模的丁肝3期临床研究 , 主要终点是考察48周治疗结束时的HDVRNA水平下降≥ 2 log和ALT正常化的复合终点 。 关键次要终点包括治疗48周后的组织学改善和纤维化改善 , 基于所有受试者在治疗开始和结束时进行的活检 。
D-LIVR研究跨越22个国家的116个临床站点 , 是全球现有最大规模的丁肝3期临床研究 , 现已有超过400名受试者参与D-LIVR 。
Lonafarnib是一款在研特征明确的一流口服异戊二烯化抑制剂 , 作用机理方面 , 它能够可阻断丁肝病毒组装的最后一个步骤 。 Lonafarnib已获得美国食药管理局FDA和欧洲药品管理局EMA的孤儿药指定、FDA快速通道指定和突破性疗法资格 。
二、完成D-LIVR注册 , 对全球丁肝药物现状影响
来自Eiger公司的总裁兼首席执行官 David Cory点评:D-LIVR研究是一项针对丁肝病毒感染的3期临床试验 , 该试验将产生关键结果 , 支持在美国、欧洲和世界其他地区批准两种针对HDV的Lonafarnib方案 。 完成D-LIVR研究注册工作 , 对于Eiger公司和慢性HDV感染患者来说是一个重要的里程碑 。 Lonafarnib可能为慢性HDV感染患者带来新治疗选择 。
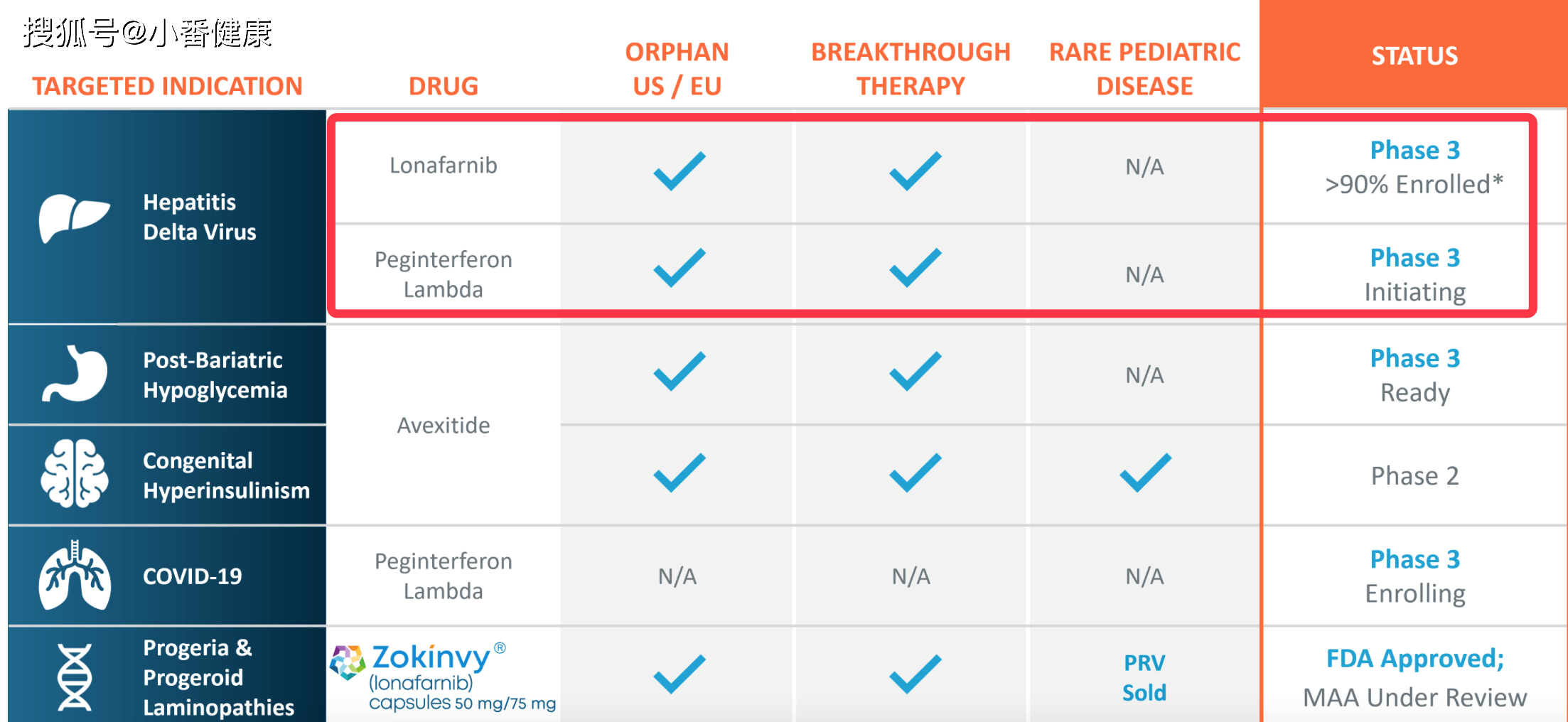
来自:Eiger公司新药研发管道 , 可见红色备注为两种在研HDV药物均在3期研究
文章图片
从新药开发管道来看 , Eiger公司正有两款都是针对HDV感染的互补疗法处在3期临床研究 , 包括Lonafarnib , 这是一种口服异戊二烯化抑制剂和聚乙二醇干扰素Lambda , 这是一种III型耐受性良好的干扰素 。
丁肝病毒感染 , 仅发生在乙肝病毒合并感染背景下 , 相比单纯乙肝病毒感染 , 丁肝可导致更严重的肝脏疾病 , 并与加速肝纤维化、HCC和肝衰竭有关 。 以往 , 全球针对丁肝病毒感染治疗药物是核苷(酸)类似物(NAs) , NA疗法仅能够抑制HDVRNA水平 , 并不会影响乙肝表面抗原(HBsAg)水平 , 无法对HDV产生影响 。 基于HDV药物现状 , 科学家积极开发HDV创新药物来满足这一领域医疗需求 。
文章图片
三、Lonafarnib是全球唯一正在开发口服HDV在研新药
小番健康结语:在D-LIVR研究中 , 两种用于HDV感染不同方案包括全口服Lonafarnib联合利托那韦和联合聚乙二醇干扰素 , 这项3期临床研究预计将在2022年底发布顶线数据 。
核心内容梳理:Lonafarnib是全球唯一正在开发用于HDV的口服药物 , 最近 , Eiger公司完成了一项3期临床研究D-LIVR的注册工作 , 这是全球最大规模的HDV 3期研究 , 已有超400名受试者参加了这项研究 , 研究将在2022年底发布数据 。
【美国|丁肝在研创新药Lonafarnib,口服抑制剂,完成3期D-LIVR注册】和美国吉利德科学的丁肝新药Bulevirtide主要区别是 , Bulevirtide是一款通过皮下注射给药的一流病毒进入抑制剂 , 而Lonafarnib是一款口服研究性异戊二烯化抑制剂 。
- 潜伏在我们身边的这3种“致癌”蔬菜,看完你还敢继续吃吗?
- 健康生活 薯条一个月最多吃两次
- 亿健H7|冬天户外空气差,不妨在家动起来!——亿健H7智能磁控划船机体验分享
- 猪油渣能不能吃?健不健康?很多人都不明白,现在知道还不晚
- 护发|吃“猕猴桃”好处多多,但有3类人不能多吃,现在知道还来得及!
- 检测|刚刚,溯源结果公布!在国际快递中检测出阳性
- 亚硝酸盐|你真的会喝水吗?喝错水的人不少,4个错误你还在犯吗?
- 水果|过年水果选哪些?这些优质年货,在你的购物清单上吗?
- 中国雄安官网1月14日电(李元闯)在雄安新区安新县|家乡雄安丨杨宏记:村民致富路上的“带头人”
- 医保|昔日近70万一针的诺西那生钠注射液纳入医保 “天价药”在临沂打出第一针
