细胞|CCR:PD-1/PD-L1一相逢,便胜却其他标志物!
近年来 , 免疫疗法在癌症治疗领域大放异彩 。
其中 , PD-1/PD-L1抑制剂无疑是最大赢家 。 不过 , PD-1/PD-L1抑制剂也一直被诟病治疗有效率不高 , 对于肺癌的客观有效率不足30% 。
如何将免疫检查点抑制剂更加精准的用于患者 , 也成为科学家研究的重心之一 。
通过免疫组化来定量PD-L1是目前最广泛被验证和使用的生物标志物 , 用于预测患者是否可以从PD-1/PD-L1抑制剂治疗中获益 。 不过 ,由于PD-L1表达的异质性 , 仍然有相当多PD-L1低表达的患者可以从该治疗上获益 , 反过来在PD-L1高表达的患者中治疗有效率也有限[1] 。 所以我们需要探索更好的生物标志物 。
近日 , 美国耶鲁大学医学院的David L. Rimm领衔的研究团队在 Clinical Cancer Research 期刊发表重要研究成果[2] 。
他们发现 PD-1/PD-L1共定位评分与非小细胞肺癌(NSCLC)患者PD-1/PD-L1抑制剂治疗获益相关 , 或许能取代传统的PD-L1的TPS评分 , 成为更有效的预测标志物 。

文章图片
论文截图
PD-1和PD-L1在肿瘤微环境中的不同细胞表达 , 它们相互作用可以传导抑制性的信号 , 使T细胞攻击肿瘤细胞的能力降低 。 PD-1/PD-L1抑制剂就是通过阻止PD-1与PD-L1相遇 , 恢复T细胞对肿瘤细胞的杀伤力[3] 。
近年来 , 科学家通过对PD-1/PD-L1空间关系的研究 , 发现 PD-1/PD-L1邻近程度与PD-1/PD-L1抑制剂疗效具有相关性[4-6] 。 最近 , Sa?nchez-Magraner团队采用荧光共振能量转移(FRET)技术评估PD-1/PD-L1相互作用 , 同样发现 接受免疫检查点抑制剂治疗的黑色素瘤和NSCLC患者总生存期(OS)与PD-1/PD-L1相互作用相关[7] 。
研究人员猜想当细胞与细胞之间靠的比较近 , 也就是PD-1/PD-L1共定位 (指不同荧光发出的颜色占据图像中的相同像素)评分较高的时候 , 而不仅仅是PD-L1高表达 , PD-1/PD-L1抑制剂可以更有效的发挥抗肿瘤作用 。
为了解决这个问题 , Rimm团队对耶鲁纽黑文医院154名NSCLC患者的肿瘤组织微阵列(TMA)进行分析 。 所有的肿瘤TMA是先前分两批制作的 , 标号分别为YTMA 404和YTMA 471 。 这些患者都接受过PD-1/PD-L1抑制剂治疗 。

文章图片
QIF估算PD-1/PD-L1的共定位评分
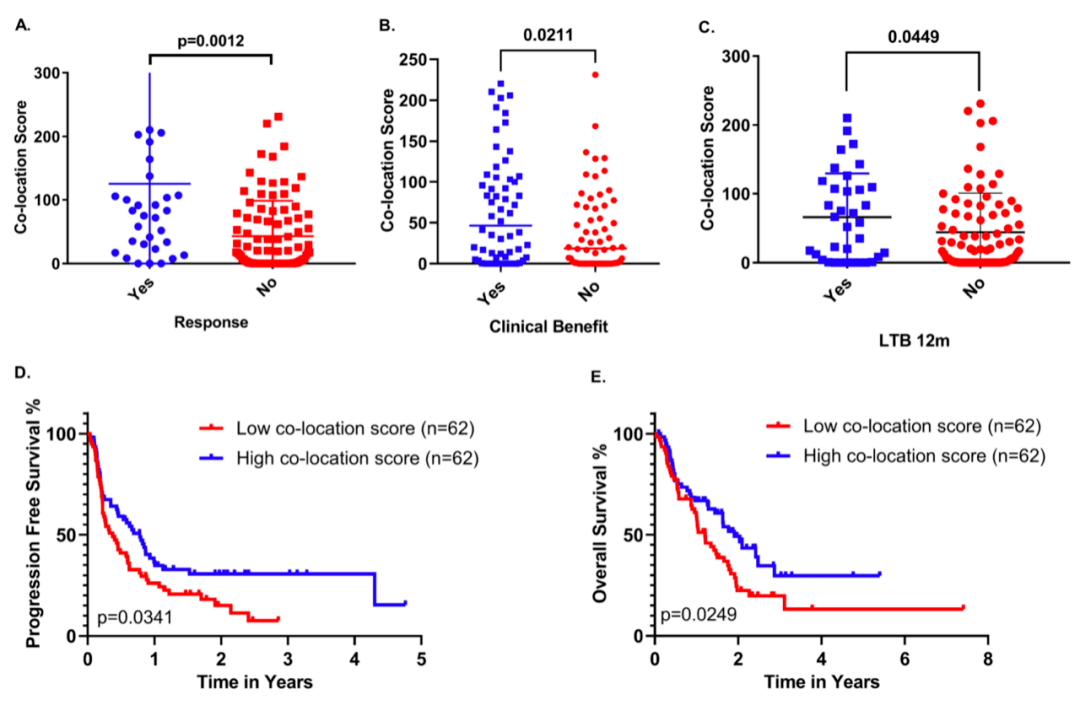
研究人员评估了124名患者肿瘤组织PD-1/PD-L1共定位评分 。 接下来 , 依据最佳疗效(BOR)将患者分为有疗效组(CR , PR;30人)与无疗效组(SD , PD;91人) 。 与 无疗效组相比 , 有疗效组明显具有更高的共定位评分(p=0.0012) 。 此外 ,持久临床获益(p=0.0211)与长期获益(p=0.0449)也均与更高的共定位评分相关 。
患者的PD-1/PD-L1共定位评分在0到231之间 , 研究人员进一步将共定位评分中位数设置为cutoff值 , 共定位评分低于cutoff值的患者被分为低评分组(62人) , 高于cutoff值的患者被分为高评分组(62人) 。 结果显示 ,患者更长的OS(p=0.0249)和PFS(p=0.0341)均与PD-1/PD-L1共定位评分高相关 。
文章图片
PD-1/PD-L1共定位评分与接受免疫治疗患者的疗效、临床获益、长期临床获益(>12月)、更长的OS和PFS相关
既往有研究发现 , 与化疗相比 , PD-1/PD-L1抑制剂作为二线及以上治疗对于NSCLC患者具有更好的疗效[8] 。 那么 , 对于PD-1/PD-L1抑制剂一线或者二线及以上治疗 , PD-1/PD-L1共定位评分表现又是怎样呢?
在本研究中 , 69名患者(44.8%)接受PD-1/PD-L1抑制剂一线治疗 , 另外85名患者(55.2%)接受PD-1/PD-L1抑制剂二线及以上治疗 。 有意思的是 ,在接受二线及以上治疗的患者中 , 共定位评分与持久临床获益相关(p=0.0147) , 在接受一线治疗的患者中却没有发现相关性 。 这是一个极具价值的发现 , 当然还需要扩大样本量来排除误差 。
- 按摩|你知道吗?间充质干细胞可以改善失眠症状
- 肝细胞|夏季来了,多吃以下3种食物,滋养皮肤,也可以淡化斑点
- 肝细胞|想长寿先养肝,多吃三种蔬菜,养肝护肝,滋补身体,脸色更红润
- 造血干细胞移植|保留脐带血,要还是不要?血液病专家告诉你答案,不用纠结了
- 肝细胞|肝不好的人,记住多喝3水,少吃1物,肝病会悄悄溜走
- 急性淋巴细胞白血病|告别“不治之症”时代,新型疗法正赋予白血病患儿新的生机
- 大蒜|癌细胞害怕什么?医生列出清单,洋葱和大蒜未上榜,该看看了?
- 这些食物能杀死癌细胞 越吃越年轻
- 小儿推拿|医生提醒:四种食物会“唤醒”癌细胞,尽量少碰,别给癌症留机会
- 红细胞|尿毒症不是“一蹴而就”,若有3种迹象,就要留心肾脏健康了
