一般而言 , 饥饿能够减少动物对环境的害怕 , 从而促进动物的猎食 。 不过 , 研究者却发现 , SRC-2基因敲除小鼠 , 就算知道外面有食物 , 也会因为害怕而不去觅食 。
显然 ,POMC神经元的SRC-2能通过调节动物的情绪促进觅食 。
【食物|《细胞》子刊:贝勒医学院徐勇团队发现SCR-2调节动物对禁食和营养过剩的适应性】
文章图片
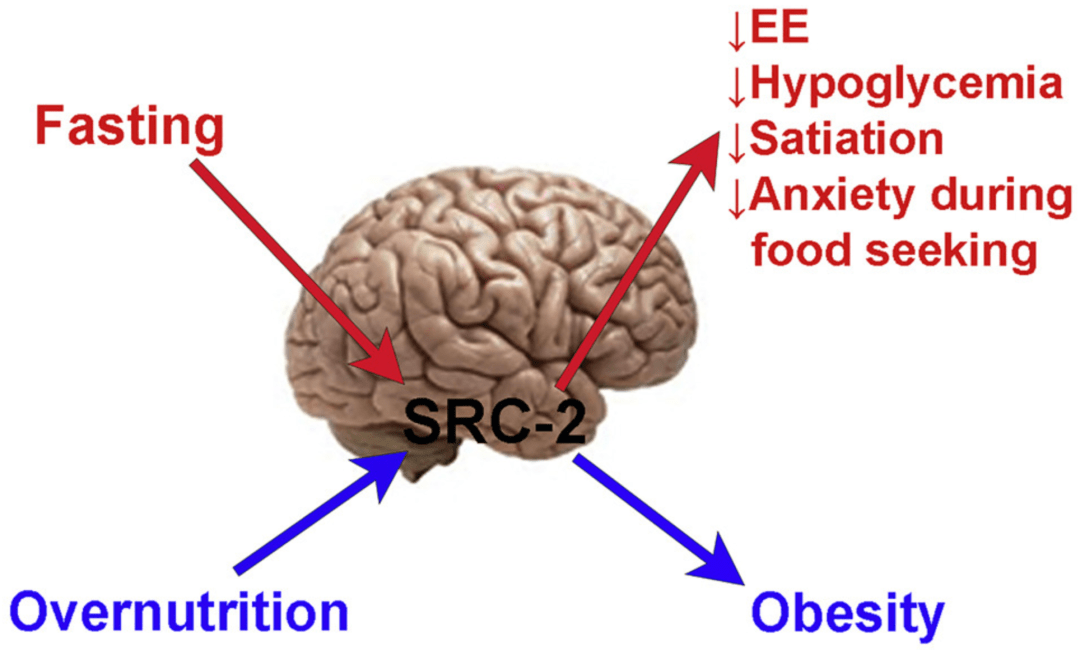
机制示意图
最近 , 代谢的调节与情绪的关联越来越受到研究人员的重视 。 该研究组曾报道 POMC神经元能够调控多巴胺神经元的活性 , 并调节与抑郁相关的饮食行为(Qu et al., 2020) 。 但是POMC神经元的SRC-2是通过哪些神经回路来调节动物在饥饿状态下对环境的害怕情绪 , 目前还不清楚 。
此外 , 研究者通过注射2-DG来模拟机体对低血糖的反应性 。 他们发现 , SRC-2基因敲除小鼠对低血糖引起的逆调节反应 , 也就是体内葡萄糖的形成 , 明显的弱于正常小鼠 。 这说明 POMC神经元的SRC-2能够帮助动物适应饥饿以及周围环境 。
研究人员还发现 ,SRC-2基因敲除的小鼠能够明显地抵抗高脂高热量食物引起的肥胖 , 而有SRC-2的正常老鼠则显现得更容易肥胖 。
显然 , 在食物充足的现代社会 , SRC-2的功能可能对人体的健康是不利的 , 而研发针对SRC-2的特异性小分子药物 ,抑制SRC-2 的功能 , 则可能成为控制现代人类“富贵病”的新手段(O'Malley, 2020) 。
贝勒医学院的杨永杰博士为本文第一作者兼共同通讯作者 , 贝勒医学院的徐勇博士为本文的通讯作者 。 其他参与研究者还包括贝勒医学院Makoto Fukuda博士 ,徐建明博士 , 孙正博士 , 和Bert W O’Malley博士 , 以及德州州立大学健康研究中心休斯顿校区(UT Health Science Center at Houston)童青春博士等 。
参考文献:
Ahima, R.S., Prabakaran, D., Mantzoros, C., Qu, D., Lowell, B., Maratos-Flier, E., and Flier, J.S. (1996). Role of leptin in the neuroendocrine response to fasting. Nature 382, 250-252.
Burnett, C.J., Li, C., Webber, E., Tsaousidou, E., Xue, S.Y., Bruning, J.C., and Krashes, M.J. (2016). Hunger-Driven Motivational State Competition. Neuron 92, 187-201.
Duerrschmid, C., He, Y., Wang, C., Li, C., Bournat, J.C., Romere, C., Saha, P.K., Lee, M.E., Phillips, K.J., Jain, M., et al. (2017). Asprosin is a centrally acting orexigenic hormone. Nature medicine 23, 1444-1453.
O'Malley, B.W. (2020). SRC-2 Coactivator: a role in human metabolic evolution and disease. Mol Med 26, 45.
Padilla, S.L., Qiu, J., Soden, M.E., Sanz, E., Nestor, C.C., Barker, F.D., Quintana, A., Zweifel, L.S., Ronnekleiv, O.K., Kelly, M.J., et al. (2016). Agouti-related peptide neural circuits mediate adaptive behaviors in the starved state. Nature neuroscience 19, 734-741.
Qu, N., He, Y., Wang, C., Xu, P., Yang, Y., Cai, X., Liu, H., Yu, K., Pei, Z., Hyseni, I., et al. (2020). A POMC-originated circuit regulates stress-induced hypophagia, depression, and anhedonia. Molecular psychiatry 25, 1006-1021.
Romere, C., Duerrschmid, C., Bournat, J., Constable, P., Jain, M., Xia, F., Saha, P.K., Del Solar, M., Zhu, B., York, B., et al. (2016). Asprosin, a Fasting-Induced Glucogenic Protein Hormone. Cell 165, 566-579.
Stashi, E., York, B., and O'Malley, B.W. (2014). Steroid receptor coactivators: servants and masters for control of systems metabolism. Trends in endocrinology and metabolism: TEM 25, 337-347.
Vella, K.R., Ramadoss, P., Lam, F.S., Harris, J.C., Ye, F.D., Same, P.D., O'Neill, N.F., Maratos-Flier, E., and Hollenberg, A.N. (2011). NPY and MC4R signaling regulate thyroid hormone levels during fasting through both central and peripheral pathways. Cell metabolism 14, 780-790.
- 鸡蛋清性|每天晚上不妨多吃三种食物,营养丰富,延缓衰老,好吃又不贵!
- 肌肤|女性不愿老太快,坚持多吃3种食物,滋补身体,好处多多!
- 排毒|女性要排毒,推荐多吃4种食物,养护皮肤,祛皱美容,血管更通畅
- 卫生室|《乡村医生诊疗口袋书(先行本)》面世
- 进行|尿毒症多半是“吃”出来的?3种食物尽量少碰,肾或许“感谢”你
- 按摩|你知道吗?间充质干细胞可以改善失眠症状
- 幽门螺杆菌的“源头”找到了,奉劝一句:三类食物,能不碰就不碰
- 肝细胞|夏季来了,多吃以下3种食物,滋养皮肤,也可以淡化斑点
- 抗衰|人到中年,3种食物换着吃,排毒抗衰,降压降脂,增强体质
- 肝细胞|想长寿先养肝,多吃三种蔬菜,养肝护肝,滋补身体,脸色更红润
