
文章图片
文章图片

非酒精性脂肪性肝炎(NASH)是一种除酒精外由其他各种因素导致的肝细胞内脂肪堆积和肝小叶内炎症为特征的临床病理综合征 , 由非酒精性脂肪肝病(NAFLD)进展而来 , 并可发展成肝硬化甚至肝癌 。
图源网络 , 如有侵权请联系作者删除
目前全球已经有超过1亿非酒精性脂肪性肝炎患者 , 他们的肝硬化和肝癌风险显著升高 。 据最新数据显示 , 非酒精性脂肪性肝炎(NASH)已成为我国慢性肝病的主要病因之一 , 严重影响着公众的健康 。
治疗非酒精性脂肪肝炎(NASH)的药物研发难度大 , 进展缓慢 , 一直被视为研发行业的黑洞 。 近年来 , 虽然针对非酒精性脂肪肝炎(NASH)的靶向药物研究取得了积极进展 , 但是 , 该病尚无获批的针对性疗法 。 今年 , 非酒精性脂肪肝炎(NASH)患者们终于看到了希望 。
据2023年9月13日消息 , 美国FDA已受理瑞司美替罗(resmetirom)治疗伴有肝纤维化的非酒精性脂肪性肝炎(NASH)成年患者的新药申请(NDA) , 并授予其优先审评资格 , 美国FDA完成新药上市申请审批的截止日期为2024年3月14日 。
据悉 , 瑞司美替罗的上市申请于2023年7月中旬向美国FDA提交 , 用于治疗伴肝纤维化的非酒精性脂肪性肝炎(NASH)成人患者 。 此时 , 距离上市申请的提交仅仅过去两个月时间 。
瑞司美替罗是一种每日一次的口服甲状腺激素受体(THR)-β选择性激动剂 。 在关键性3期MAESTRO-NASH系列试验中 , 瑞司美替罗同时实现了肝组织学改善终点——非酒精性脂肪性肝炎的消退和肝纤维化的减轻 。
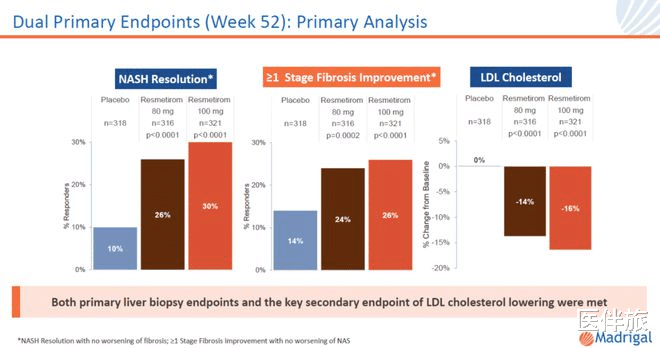
研究结果显示 , 两个给药组达到52周主要终点非酒精性脂肪性肝炎消减的比例分别为26%及30% , 安慰剂组为10%;两个给药组达到52周主要终点纤维化改善的比例分别为24%及26% , 安慰剂组为14% 。 (见图一)
图一
此外 , 瑞司美替罗还达到试验的多项次要终点 , 显著降低多种脂质、脂蛋白、低密度脂蛋白胆固醇(LDL-C)指标 。 在关键次要终点上 , 80 mg给药组在24周的低密度脂蛋白胆固醇(LDL-C)平均改变为 -12% , 100 mg组为 -16% , 而安慰组的改变为平均1% 。 (见图二)
【肝脂肪降低51%!瑞司美替罗上市申请获FDA优先审评资格】图二
利用基于核磁共振的无创检测手段对肝脏脂肪水平的评估显示 , 接受瑞司美替罗100 mg治疗52周后 , 患者肝脏脂肪水平平均降低51% 。 肝纤维化、肝脏体积和脾脏体积也显著降低 。 (见图三)
图三
安全性方面 , 与安慰剂组相比 , 瑞司美替罗组报告的最常见不良事件(频率更高)是治疗开始时出现的一般轻微且短暂的腹泻和恶心 。
参考资料:
1.Madrigal Pharmaceuticals Announces NDA Acceptance and Priority Review of the New Drug Application for Resmetirom for the Treatment of NASH with Liver Fibrosis. Retrieved September 13 2023 from
https://ir.madrigalpharma.com/news-releases/news-release-details/madrigal-pharmaceuticals-announces-nda-acceptance-and-priority.
2.Madrigal Announces Positive Topline Results from the Pivotal Phase 3 MAESTRO-NASH Clinical Trial of Resmetirom for the Treatment of NASH and Liver Fibrosis. Retrieved September 13 2023 from https://ir.madrigalpharma.com/news-releases/news-release-details/madrigal-announces-positive-topline-results-pivotal-phase-3.
- 肝病别拖延,若是上厕所出现这3种现象,或许是肝受损了
- 帕梅拉火爆Youtube徒手训练,堪称脂肪杀手
- JAMA:斑块缩小1%,就可显著降低心血管风险!做好3点,或可“逆转”斑块
- 胸膜炎、肝腹水、肾性水肿,一个“千古”良方,4味中药保驾护航
- 4个减脂餐原则,降低热量摄入,让你不知不觉瘦下来
- 经常放屁就是肝不好?出现2个症状需警惕,或是疾病预兆
- 肝变硬,头先知?医生提醒:头部若出现这3种情况,建议重视起来
- 研究速递:老年人每天走够这些步,降低近一半心脑血管风险!
- WHO发布新指南:脂肪、碳水化合物怎么吃更健康?
- 多吃素也可能得脂肪肝?脂肪不是最大威胁,揭示4大被忽略的元凶
