Peinado|《自然》子刊:癌细胞转移前就把“黑手”伸进了淋巴管!科学家发现,黑色素瘤细胞会释放外泌体改造淋巴管,促进肿瘤转移丨科学大发现( 二 )
文章图片
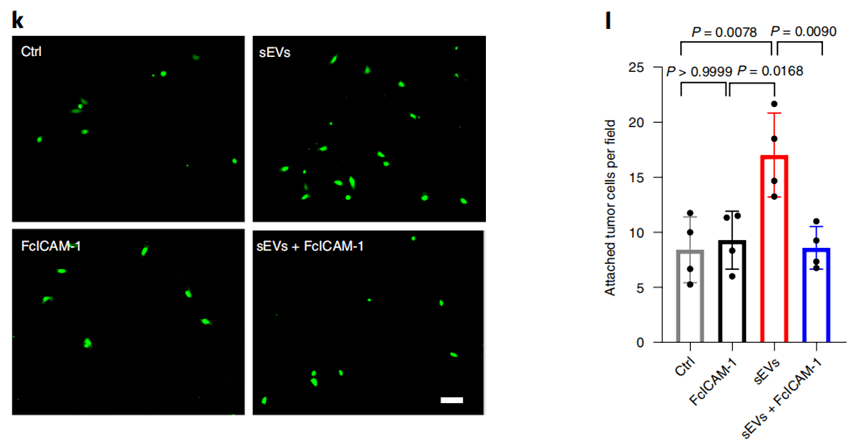
LECs吃了外泌体变粘了 , 和ICAM-1脱不了干系
另一方面 , 外泌体还会促进LECs增殖 , 导致淋巴管分支增多 , 而淋巴管生成也正是肿瘤在转移到淋巴结前诱导免疫抑制环境的重要环节 。
研究者们观察到 ,LECs在吸收外泌体的48h后 , 淋巴管生成和血管生成相关信号(LYVE1 , VEGFC , VEGFR3等)发生富集 。当用B16-F1R2细胞释放的外泌体处理LECs时 , 24h后LECs便可增殖达3.5倍 。
文章图片
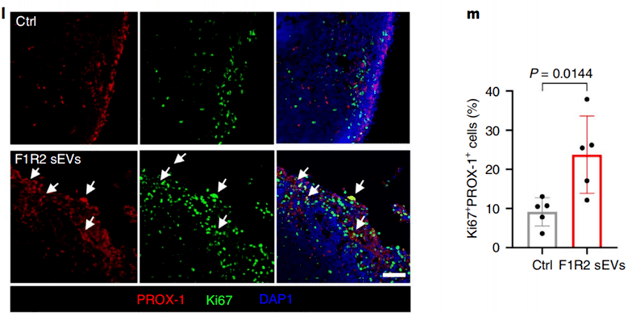
LECs吃了外泌体 , 长势大好
值得注意的是 , 已有研究证明淋巴结处的巨噬细胞会分泌淋巴管生成因子[6] 。 但在这里 , 并没有观察到巨噬细胞在吸收外泌体后 , 淋巴管生成因子水平有任何变化 。 反倒是发现 , 这些巨噬细胞有抑制淋巴管异常生长的作用 。
也就是说 ,黑色素瘤细胞释放的外泌体会先行到达淋巴结处 , 在那里被LECs吸收后 , 便开始指挥LECs卖苦力 , 为黑色素瘤的转移打造适宜的微环境 。
那么 , 外泌体又是如何“威胁”LECs为自己所用呢?
Peinado和他的团队首先想到NGFR 。 这是一种神经生长因子受体 , 已有研究发现 ,NGFR与黑色素瘤转移、角膜炎症过程中的淋巴管生成相关 , 而且NGFR在黑色素瘤细胞中的表达水平高于其他类型的肿瘤细胞[7-9] 。
巧的是 , 一系列研究发现 ,外泌体不仅能够诱导LECs中 Ngfr 转录水平上调 , 还会在LECs中释放自己的NGFR , 最终导致LECs内的NGFR总体水平上调。 而且 ,只有高转移水平的黑色素瘤细胞释放的外泌体才含有NGFR , 而在低转移水平的黑色素瘤细胞释放的外泌体中几乎没有NGFR 。
通过CRISPR技术、蛋白质组学分析等技术 , 研究者们发现 , 黑色素瘤细胞中的NGFR水平降低后 , 所释放的外泌体中蛋白组分也发生变化 , 包括NGFR在内的126种蛋白质水平显著下调 ,281种蛋白质水平显著上调 。
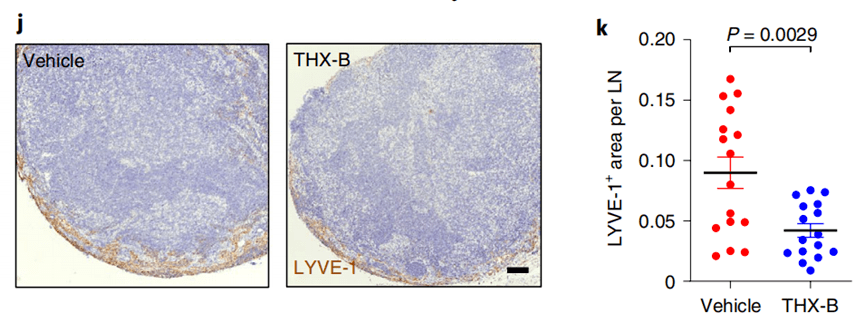
进一步研究结果显示 ,由外泌体分泌的NGFR会诱导LECs中的MAPK和NF-κB通路 , 从而促进肿瘤细胞黏附和淋巴管生成 。当用NFGR抑制剂 (THX-B)来治疗黑色素瘤小鼠时 , 小鼠的黑色素瘤转移情况得到缓解 。
文章图片
只用NGFR抑制剂后 , 小鼠淋巴管分支增长情况得到缓解
既然在小鼠中确定 ,外泌体中NGFR的表达和活性是关键一环 , 那对我们人类来说呢?
Peinado和他的团队通过对人类癌症基因组图谱(The Cancer Genome Atlas)的数据进行分析发现 ,与原发性黑色素瘤相比 , NGFR表达水平在转移性黑色素瘤中显著增加 。
这一点在III/IV期黑色素瘤患者的组织学分析中也得到了证实 。组织活检结果显示 , 与原发肿瘤相比 , 已发生黑色素瘤转移的淋巴结组织中 , NGFR表达水平更高 。
研究者们还证实 ,淋巴结组织活检中NGFR + 细胞的数量能够用来预测黑色素瘤患者的生存情况。
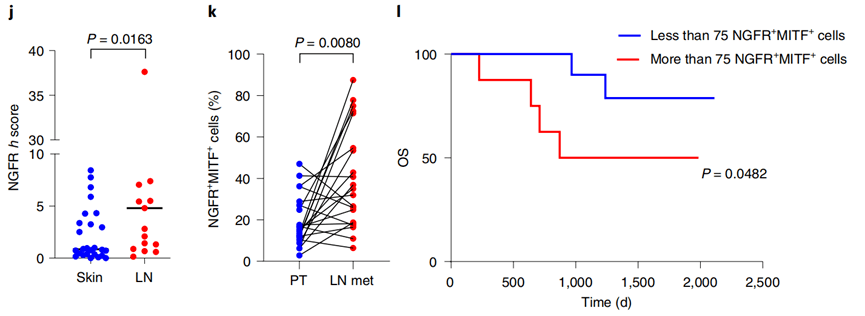
文章图片
NGFR可以作为黑色素瘤进展和早期诊断的重要生物标志物
总的来说 , Peinado和他的团队发现 , 黑色素瘤细胞能够释放携带有NGFR的外泌体到淋巴结 , 诱导淋巴管分支生成、增强淋巴管内皮细胞与黑色素瘤细胞的粘附作用 , 从而促进黑色素瘤的转移 。
在本次研究中 , 研究者们不仅用NGFR 抑制剂 (THX-B)成功缓解了黑色素瘤小鼠的肿瘤转移情况 ,还在黑色素瘤患者中证实 , NGFR可以作为黑色素瘤转移的有效预测靶点 。 这为对抗黑色素瘤转移的治疗提供了新策略 。
- 卫生室|《乡村医生诊疗口袋书(先行本)》面世
- 解读|《浙江省医院门诊管理办法》政策解读
- 廉东波|《健谈》观点丨浅表性胃炎三五年复查一次 萎缩性胃炎一年一查
- 家长|杭州《青少年皮肤健康状况调研》发布,近半青少年受皮肤疾病困扰
- 公报,监测,国民,体质|一图读懂《第五次国民体质监测公报》
- 感冒|《气血运行影响心脏功能——心悸篇》
- 幽门螺杆菌感染|《健谈》观点丨突然消瘦、胃痛、黑便,应及时做胃镜检查
- 数据|《胃肠病学》:减肥防早发肠癌,要从20岁开始!科学家发现,20、30岁和约45岁时肥胖,与结直肠癌发病风险上升88-156%有关
- 糖尿病|糖尿病的“福音”终于被找到了,每天吃一点,“血糖”自然降下来
- 医学|科普连载:《氢气医学人群试验》(漫画版)孙学军教授 序言
