肿瘤相关巨噬细胞(TAM)富集于多种实体肿瘤中 , 它是 肿瘤微环境中的头号叛军 , 也是肿瘤免疫治疗中的重要靶点[1] 。
在肿瘤免疫微环境中 , TAM主要表现为具有促肿瘤活性的M2型 。 但由于巨噬细胞具有极强的可塑性 , 科学家们发现 ,TAM可以在外界条件的刺激下 , 被极化为具有抗肿瘤活性的M1型 。 这种将TAM重编程的研究思路 , 为抗肿瘤提供了多种潜在的治疗方案[2] 。
近日 , 来自美国冷泉港实验室的Mikala Egeblad博士及其研究团队 , 在 Cancer Cell 期刊中报道了一种通过重编程TAM杀死肿瘤细胞的新方法[3] 。
他们发现 ,单磷酰脂质A(MPLA)及干扰素-γ (IFN-γ)联用 , 是一种安全有效的抗肿瘤疗法 。 该疗法一方面 将TAM重编程为具有抗肿瘤活性的M1型巨噬细胞 , 另一方面 借TAM释放的细胞因子来间接激活细胞毒性T细胞 , 从而杀死肿瘤细胞 。
值得一提的是, MPLA已被FDA批准用于疫苗的佐剂 , 而IFN-γ也已被FDA批准用于慢性肉芽肿病的治疗 。 二者在前期累积的临床使用经验和安全性数据 , 无疑会加快它们在今后合体进入临床癌症治疗的速度 。

文章图片
论文首页截图
巨噬细胞M1型的极化 , 主要依赖于Toll样受体(TLR)的激活(如脂多糖及Toll样受体激动剂等)或细胞因子(如IFN-γ)的刺激[1] 。 而MPLA就是一种靶向TLR4的脂多糖衍生物 。MPLA虽然与脂多糖有着相似的结构 , 但是MPLA在降低脂多糖毒性的同时 , 最大程度保留了脂多糖的免疫功能 。
为了验证MPLA+IFN-γ可以重编程TAM , 并使之具有抗肿瘤活性 , Egeblad博士及其团队首先以管状B型乳腺癌小鼠为模型(PyMT) , 提取了原位瘤中的肿瘤细胞及TAM , 并将其与IFN-γ及TLR受体激动剂(LPS, MPLA, 及 polyI:C)共孵育 。
他们发现 只有将IFN-γ与LPS或MPLA联用才能杀死PyMT肿瘤细胞 。
IFN-γ及TLR受体激动剂(LPS, MPLA, 及 polyI:C)与PyMT癌细胞及TAM共孵育48小时后
考虑到诱导一氧化氮合酶(iNOS)释放一氧化氮(NO) , 是巨噬细胞极化为M1型发挥抗肿瘤活性的标志之一 , 因此Egeblad博士及其团队进一步研究了MPLA+IFN-γ对TAM iNOS表达的影响 。
和他们预期的一样 ,只有IFN-γ与MPLA联用才能诱导iNOS的表达 , 而且这种诱导作用来源于 , MPLA与IFN-γ单独对iNOS编码基因Nos2的上游转录因子NF-kB及STAT1的调控 。 这为MPLA和IFN-γ联用重编程TAM在机制层面提供了解释 。
为了证明MPLA+IFN-γ可以在动物肿瘤模型中重编程TAM , Egeblad博士及其团队紧接着在转移性乳腺癌PyMT小鼠模型上进行实验 。 他们发现 ,瘤内注射MPLA+IFN-γ后 , 不仅肿瘤内巨噬细胞的占比升高了 , 表达iNOS及CD40的M1型巨噬细胞占比也显著增加 , 同时表达CD206的M2型巨噬细胞占比显著降低 。 这说明MPLA+IFN-γ可以实现对PyMT小鼠模型中TAM的重编程 。
【细胞|《细胞》子刊:让叛徒巨噬细胞回炉重造,两种老药提供新抗癌思路!】
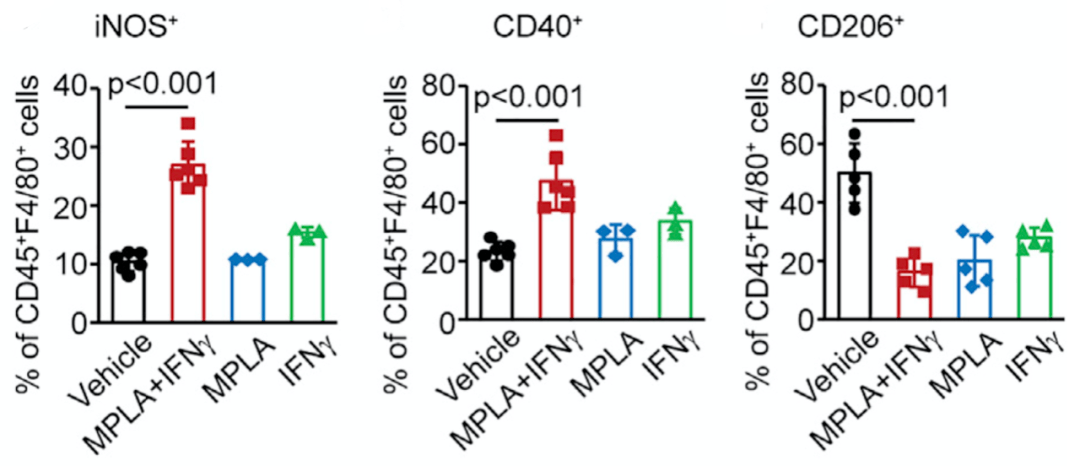
文章图片
各组iNOS+、CD40+、及CD206+巨噬细胞占比比较
同时 , Egeblad博士及其团队还从乳腺癌转移患者的恶性胸水中提取出了癌细胞及TAM , 来考察MPLA+IFN-γ对患者肿瘤细胞的作用 。
结果发现 ,MPLA+IFN-γ可以杀死80%-90%的乳腺癌患者肿瘤细胞 。 RT-qPCR分析发现 , 只有MPLA+IFN-γ联合使用可以显著升高M1型巨噬细胞的标志物(NOS2, CD40, TNF, IL12B) , 并且显著降低TAM的标志物(IL10, MRC1) 。 说明MPLA+IFN-γ也可以重编程乳腺癌转移肿瘤患者恶性胸水中的TAM 。
- 卫生室|《乡村医生诊疗口袋书(先行本)》面世
- 按摩|你知道吗?间充质干细胞可以改善失眠症状
- 肝细胞|夏季来了,多吃以下3种食物,滋养皮肤,也可以淡化斑点
- 肝细胞|想长寿先养肝,多吃三种蔬菜,养肝护肝,滋补身体,脸色更红润
- 解读|《浙江省医院门诊管理办法》政策解读
- 廉东波|《健谈》观点丨浅表性胃炎三五年复查一次 萎缩性胃炎一年一查
- 家长|杭州《青少年皮肤健康状况调研》发布,近半青少年受皮肤疾病困扰
- 造血干细胞移植|保留脐带血,要还是不要?血液病专家告诉你答案,不用纠结了
- 肝细胞|肝不好的人,记住多喝3水,少吃1物,肝病会悄悄溜走
- 公报,监测,国民,体质|一图读懂《第五次国民体质监测公报》
