约10%-15%的多发性骨髓瘤患者可并发免疫球蛋白轻链淀粉样变性 , 其特征是错误折叠的轻链(淀粉样蛋白)沉积在重要器官 , 例如淀粉样心肌病或肾病导致的重要器官受损是轻链淀粉样变性的已知并发症 。 对于存在肾病范围蛋白尿(Nephrotic-Range Proteinuria)、巨舌症、眶周瘀斑、颌下腺肿大、不明原因心肌病的多发性骨髓瘤患者 , 应考虑存在轻链淀粉样变性;此外对于具有上述特征的多发性骨髓瘤患者 , 应对骨髓和腹部脂肪进行活检以及刚果红染色以寻找淀粉样蛋白 。
诊断
实验室检查
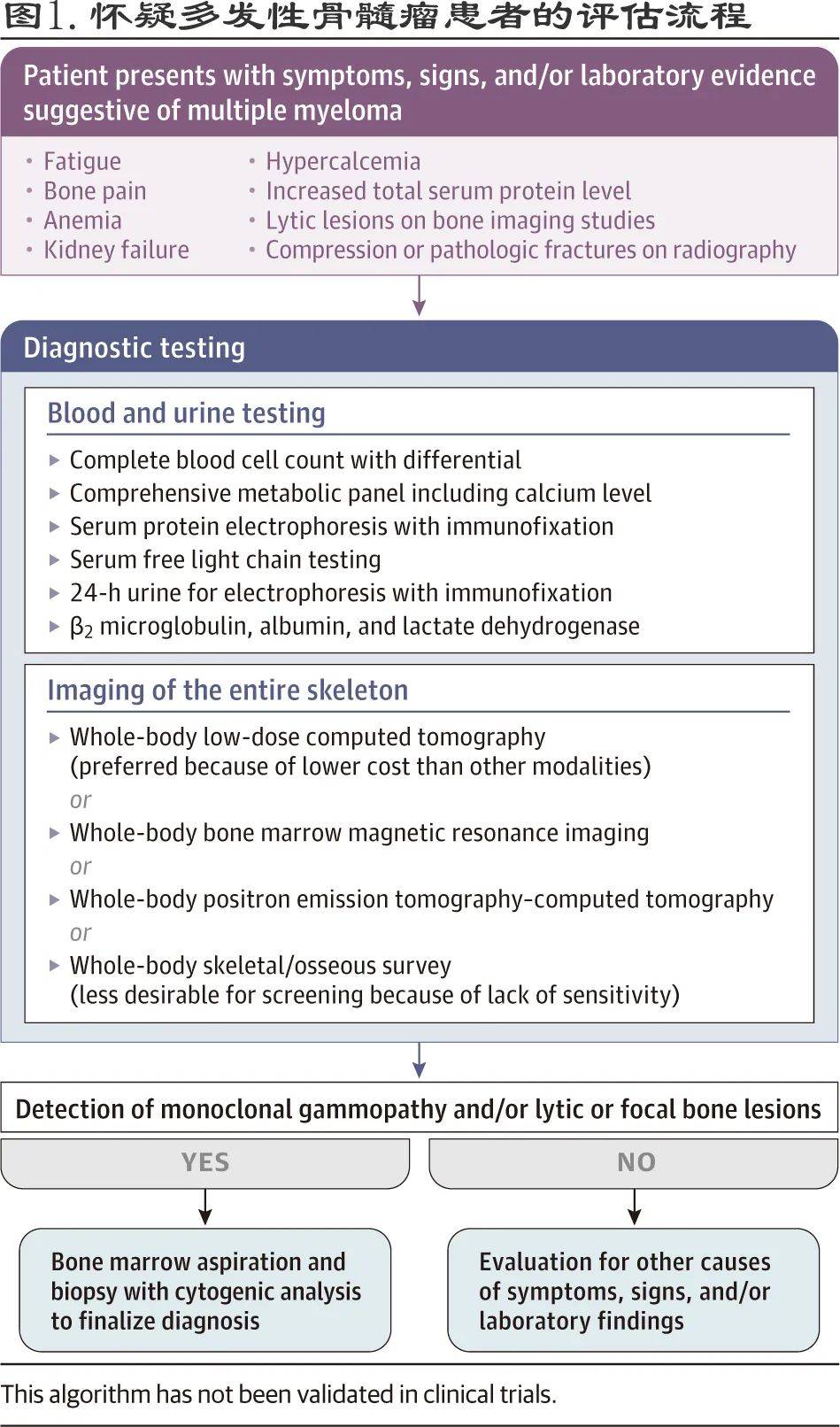
多发性骨髓瘤的实验室初始检查应包括全血细胞计数及分类、血清肌酐、血清钙、白蛋白、乳酸脱氢酶、血清游离轻链和β2微球蛋白水平、血清和24小时尿蛋白电泳及免疫固定(图1) 。
文章图片
约86%的多发性骨髓瘤患者血清蛋白电泳可检出单克隆蛋白 。 24小时尿蛋白检测定量本周氏蛋白是重要的诊断指标 , 以确定是否存在基线蛋白尿 , 并评估继发性轻链淀粉样变性 , 后者常表现为肾病范围蛋白尿;应进行血清游离轻链测定 , 因其可定量κ和λ游离轻链水平(轻链可能升高并导致终末器官损伤);记录基线时单克隆蛋白和血清游离轻链的数量对于评估基线疾病的程度和治疗响应非常重要 , 监测单克隆蛋白和游离轻链水平随时间的变化可确定治疗是否成功 。
此外 , 约有1%-2%的患者无可测量的血清或尿液标志物 , 称为“非分泌性”多发性骨髓瘤 。
如果怀疑浆细胞白血病 , 应考虑使用流式细胞术来识别异常的循环浆细胞 。 怀疑多发性骨髓瘤的所有患者均应进行单侧骨髓穿刺和活检;分析骨髓(包括浆细胞形态学);通过免疫组织化学、流式细胞术、荧光原位杂交(FISH)和常规细胞遗传学对组织芯活检中的CD138+浆细胞进行定量 。
新诊断的多发性骨髓瘤均应进行基线全身低剂量 CT、MRI或PET-CT影像学检查 , 影像学可证实压缩性骨折、溶骨性病变或病理性骨折 。 如果不可行 , 可考虑骨检查 。
诊断多发性骨髓瘤必须满足以下标准:骨髓中克隆性浆细胞≥10% , ≥1个典型实验室或放射学多发性骨髓瘤症状(高钙血症、肾脏受累、贫血和骨病变[“CRAB”])证实存在明显的终末器官损害(表1) 。 2014年 , 国际骨髓瘤工作组扩展了需要治疗的活动性或症状性多发性骨髓瘤的诊断标准 , 纳入了“骨髓瘤生物标志物” , 例如 , 骨髓骨髓浆细胞≥60%、受累/未受累游离轻链比值≥100、磁共振成像(MRI)下>1个≥5mm局灶性病变 。 因此 , 多发性骨髓瘤的确诊标准为:在骨髓中有10%或以上异常浆细胞和至少1个终末器官事件(CRAB标准)或骨髓瘤生物标志物 , 如表1所示 。
影像学
骨性终末器官损伤包括可导致病理性骨折的溶骨性骨病变 , 它很常见并导致显著的发病和死亡 。 诊断时 , 70%的多发性骨髓瘤患者存在骨性终末器官损伤 。 并且骨和骨外浆细胞瘤(浆细胞肿瘤样生长)也可在基线影像学中证实 。 此外影像学对评估新诊断或复发的多发性骨髓瘤患者溶骨性骨病和浆细胞瘤的范围也具有重要意义
CT或PET-CT是诊断多发性骨髓瘤的首选方法 , 如果SMM患者临床高度怀疑多发性骨髓瘤时应考虑CT或PET-CT 。 CT扫描可用于检测多发性骨髓瘤、SMM和MGUS患者的溶解性病变 , 其检出率高于普通X线 。 PET-CT可评估多发性骨髓瘤骨和骨外表现的存在、范围和代谢活性 。
MRI是多发性骨髓瘤的替代影像学模式 , 目前关于区分SMM和需要治疗的多发性骨髓瘤的共识指南均推荐CT作为SMM患者的初始诊断工具 , 但如果结果为阴性 , CT后应进行MRI检查以寻找骨髓中≥1个局灶性病变 。 在一项149例SMM患者的研究中 , 当MRI显示存在1处以上局灶性病变时 , 在中位随访13个月时即进展为需要治疗的多发性骨髓瘤 , 而MRI上无局灶性病变的患者在43个月时仍未达到中位至进展时间 。 此外MRI也可用于随访接受治疗的患者 , 以确定疾病复发或监测治疗响应 。
- 治疗|癌症晚期患者:死亡都是一种奢侈,真的太痛了!癌痛到底有多痛?
- 神经细胞|中科西部干细胞研究院:“干细胞”有望成为中风最好治疗方式!
- 症状|李俊才:运动神经元病怎么治疗能够达到控制病情?
- 团队|我国科学家在干细胞治疗糖尿病研究中获得重要进展!
- 团队|我国科学家在干细胞治疗糖尿病研究中获得重要进展
- 脂肪酸|肠道菌群紊乱还会引起糖尿病?如何治疗才最有效?解决方案来了!
- 治疗|提醒:真正对降糖有帮助的,只有这5个方法!
- 血管|体检查出这3种肝脏疾病,不要病急乱投医,以免过度治疗
- 治疗|乙肝新药NASVAC,已在国外注册免疫药物,研发走多学科合作之路
- 简单按摩体操 治疗痛经
