目前 , 对于无法手术的晚期肺癌患者 , 如果一线治疗驱动基因阴性且PD-L1高表达 , 指南会推荐患者接受单独免疫治疗或免疫治疗联合化疗[1] 。
既往有研究显示 , 对于 接受免疫治疗的患者 , 患者的基线体重指数(BMI)升高与患者的总生存获益相关[2] 。 同时 , 也有学者发现 ,BMI的这种预后改善作用在单纯化疗组并未显示[3] 。
这说明BMI升高的预后改善作用可能是通过增强免疫治疗的疗效而达到的 。 那如果患者接受免疫联合化疗 , 还会有这种预后改善作用吗?
为回答此问题 ,英国伦敦帝国理工学院外科与癌症研究所的Alessio Cortellin团队开展了一项国际多中心回顾性研究[4] 。 他们发现 ,在接受免疫联合化疗的晚期非小细胞肺癌患者中 , 体重指数(BMI)对患者的无进展生存期(PFS)和总生存期(OS)没有影响 。 相关研究成果发表在著名期刊 The Journal for ImmunoTherapy of Cancer(JITC) 上 。

文章图片
▲ 文章题目
这个研究共纳入了2014年12月至2021年8月 , 来自全球15个研究机构共计853例IV期非小细胞肺癌患者 , 所有患者均接受了免疫治疗联合化疗 , 在治疗后患者接受了基于RECIST 1.1标准[5]的疗效评估 。 该研究的主要终点为患者的总生存期(OS)和无进展生存期(PFS) 。
按照WHO对体重指数的分组建议 , 研究人员将患者分为低体重组(BMI<18.5)、标准体重组(18.5≤BMI≤24.9) , 超重组(25≤BMI≤29.9)和肥胖组(BMI≥30) 。
考虑到不同BMI分组间的差异可能会影响最终对于OS统计分析结果 , 研究人员首先分析了不同BMI分组患者之间的临床病理信息差异 , BMI较大的患者具有更高的年龄(p=0.00085) , 该组患者的不吸烟人数(p<0.0001)及PS评分较好(p=0.0127)的比例也更高 , 而肝转移的比例更低(p=0.0395) 。
文章图片
在中枢神经系统转移方面 , 不同BMI组也有显著差异(p=0.0002) ,超重组患者具有最低的中枢神经系统转移比例(17.8%) 。 在肺癌中较为常见的KRAS突变 , 肥胖组患者中有接近一半人均伴有此类突变(41.9%) 。
在 进行单因素分析中 , 不同BMI分组之间的OS具有统计学差异(log rank: p=0.045) 。 但是 ,从低体重组到最终肥胖组的趋势分析检验未见随着体重升高引起的OS改善作用(p=0.131) 。 研究人员同时还分析了不同BMI分组的PFS差异 。 最终发现 ,不同分组之间患者的PFS无统计学差异(log rank: p=0.123, log rank test for trend: p=0.510) 。
在进行生存分析时 , 如果分组变量具有等级关系 (比如本研究的BMI从小到大的等级关系) , 我们可以通过趋势分析检验(p for trend)来确定具有等级的分组变量是否与最终的结果具有线性关系 (比如本文的随着患者BMI升高而改善OS的假设) 。
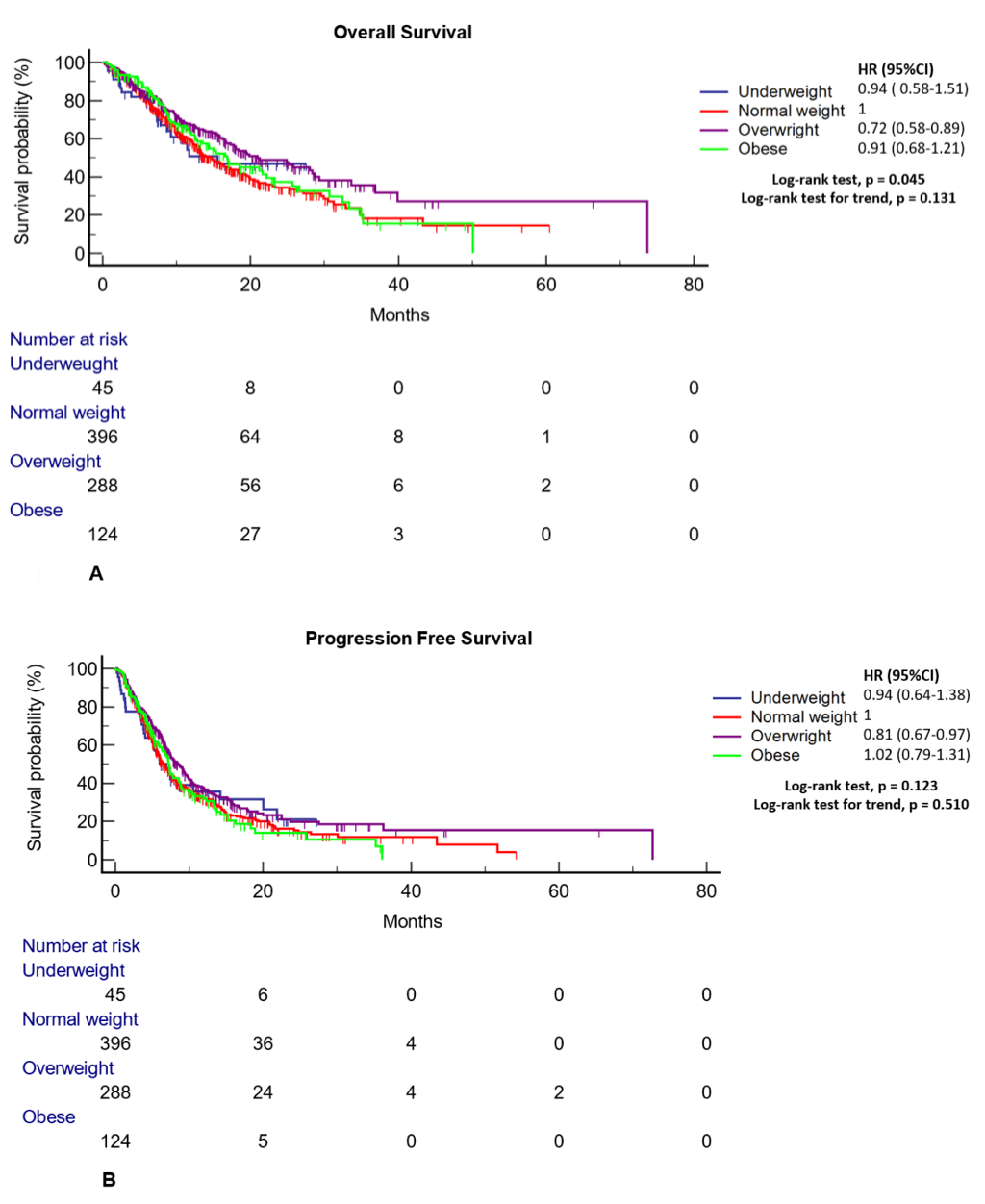
文章图片
▲ 不同BMI分组对患者OS及PFS的影响
为了调整不同BMI分组之间患者基线信息对于最终OS的影响 , 研究人员进行了多因素分析 , 发现 不同的BMI分组对PFS或OS均无影响 。
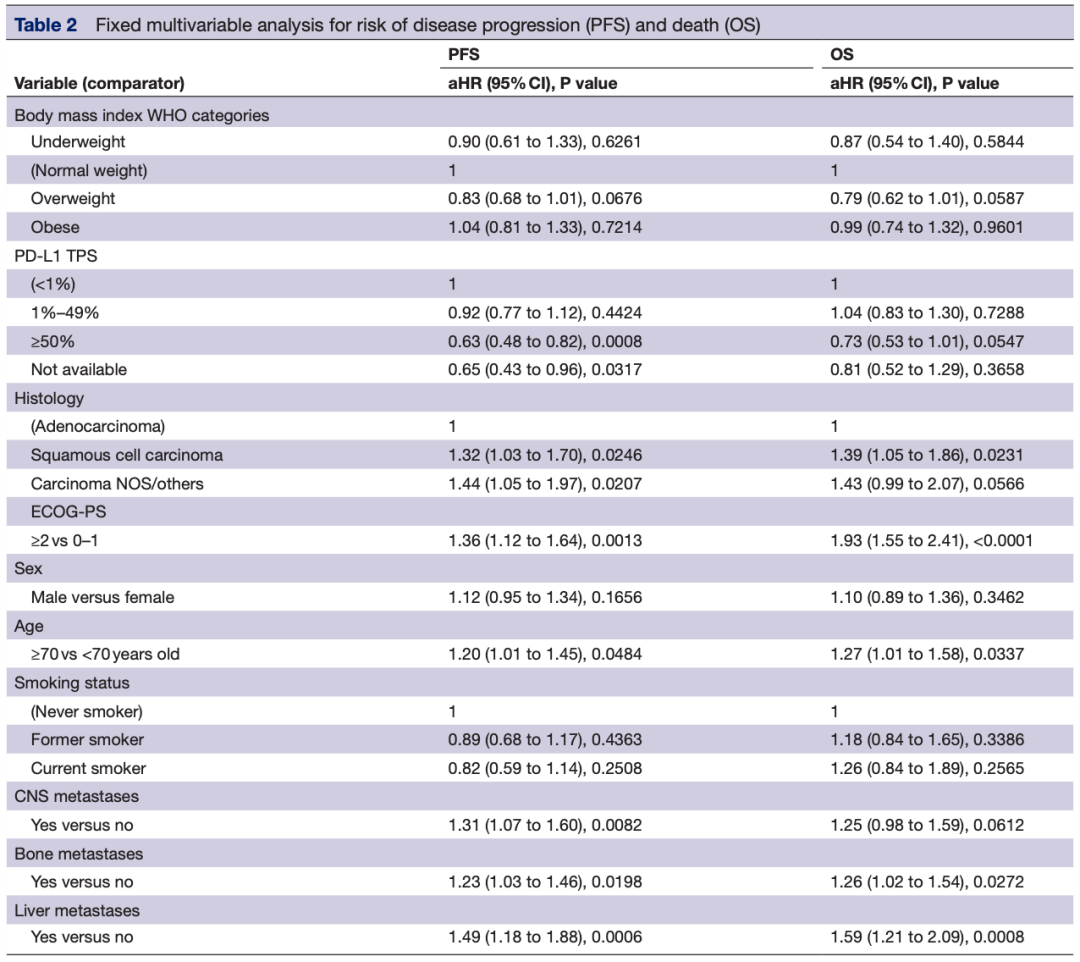
文章图片
【分组|JITC:肥胖与晚期非小细胞肺癌免疫+化疗的预后无关】▲ 多因素回归分析矫正后结果
为了探究OS及PFS的影响因素 , 研究人员对纳入患者的临床病理因素进行了多因素分析 。 经过分析发现 ,相较于BMI , 传统的临床病理因素对于患者的OS及PFS影响更大 。 研究人员发现 , 肿瘤内PD-L1表达、患者体力状态评分、原发肿瘤组织学、年龄、中枢神经系统、骨及肝转移是影响患者PFS的独立危险因素 。 而患者体力状态评分 , 原发性肿瘤组织学 , 年龄 , 骨和肝转移是影响患者OS的独立危险因素 。
- 细胞|JITC:颠覆认知!科学家首次发现PD-1抑制剂竟保护特定肠癌细胞,促进结直肠癌生存,免遭放化疗杀伤丨科学大发现
- 打呼噜|健康公开课:肥胖、不孕、抑郁...睡眠呼吸暂停的危害不可小觑!
- 初二|减重手术丨初二学生体重240斤!男孩因过度肥胖被迫休学……
- 中国医师协会|警惕肥胖找上门
- 不良的生活习惯不仅会导致肥胖、亚健康等问题|甜椒炒鸡胸肉,减肥减脂的小帮手,甜椒炒鸡胸肉减肥餐
- 运动|人到中年,代谢水平下降是肥胖的主因!掌握5点,提升代谢水平
- 本文转自:北青网早睡一定程度上能预防肥胖?是的|4天睡不好就可能增肥!早睡一定程度上能预防肥胖
- 营养|健康充电 | 肥胖更要加营养,吃的差才长赘肉!
- 中国医师协会|三餐外卖? 警惕肥胖找上门
- 中国医师协会|三餐外卖?警惕肥胖找上门
