
文章图片
文章图片

昨天介绍了由临床阶段生物制药公司(Aligos Therapeutics)自研II类衣壳组装调节剂ALG-000184组合恩替卡韦(ETV)第1期临床开发部分已发表于2023年全球肝炎峰会上(GHS-2023 , 在法国巴黎举行) , 以下是该试验的完整数据集 。
本研究出处 , 来自Aligos、GHS-2023乙肝在研新药ALG-000184 , 1期超12周组合ETV , 完整试验数据
该研究课题:使用CAM ALG-000184和ETV治疗超过12周剂量依赖性地调降慢性乙型肝炎(CHB)乙肝e抗原阳性受试者的乙肝表面抗原(HBsAg)水平 。 研究人员介绍 , 研发可产生空病毒颗粒(CAM-E)的衣壳组装调节剂已被广泛研究用于治疗CHB 。
CAM-E类候选药物 , 有两种抗病毒作用机制 , 包括抑制乙肝病毒前基因组RNA(HBV pgRNA)封装导致HBVDNA和RNA水平下降 , 并防止新的cccDNA合成 , 导致HBsAg减少 。
ALG-000184-201研究第四部分队列 , 来自Aligos目前 , ALG-000184(CAM-E的口服前药 , ALG-001075)正在进行一项随机、双盲、多部分的1期研究(ALG-000184-201)中进行评估 , 包括在初治或目前未接受治疗的CHB受试者中进行评估 。 先前已证明在给药28天后具有良好的安全性、药代动力学(PK)和有效抗病毒活性 。 正在评估更长的给药时间 , 包括在我国(第四部分的2个队列) 。 本研究提交的是使用ALG-000184+ETV ≥12周的受试者现有数据 。
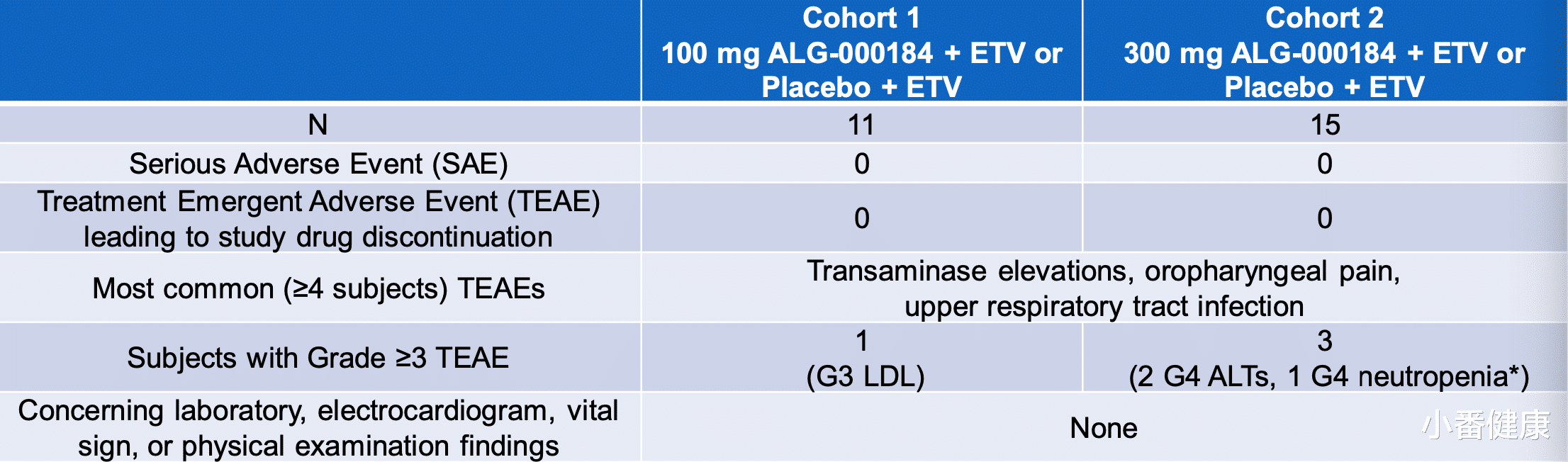
第四部分安全性方面 , 来自Aligos【乙肝|乙肝在研新药ALG-000184,1期超12周组合ETV,完整试验数据】结果表明 , 100毫克或300毫克ALG-000184+ETV具有良好的耐受性 。 第四部分队列1(100毫克ALG-00184 + ETV x 24周) , N=4 , 使用100毫克ALG-000184 + ETV x 24周 , 在第24周 , 所有受试者的HBVDNA下降都 >6 log 10 IU/ml 。 在先单用ETV后加用ALG-000184 , 与单用ETV相比 , 该组合疗法导致HBVDNA额外下降~2 log 10 IU/mL 。
第四部分队列1(100毫克ALG-00184 + ETV x 24周):接受ALG-000184 x ≥12周的受试者的HBsAg下降情况 , 来自Aligos第四部分队列1 , 在第24周时 , 4名受试者中有3名的乙肝表面抗原水平下降 >0.4 log 10 IU/ml , 乙肝表面抗原最大下降幅度~0.7 log 10 IU/ml , 添加ALG-000184以后 , 看到了乙肝表面抗原下降趋势 。
第四部分队列2(300毫克ALG-00184 + ETV x 48周):N=7和N=5 , 分别使用300毫克ALG-000184+ETV×≥12周和≥24周 , 在第24周时 , 所有受试者的HBVDNA下降 ≥ 6 log 10 IU/ml , 有1名受试者实现检测不到 。
第四部分队列2(300毫克ALG-00184 + ETV x 48周):接受ALG-000184 x ≥12周的受试者的HBsAg下降情况 , 来自Aligos12周后 , 7名有6名受试者的乙肝表面抗原下降≥0.4 log 10 IU/ml , 24周后 , 5名中有4名受试者的乙肝表面抗原下降≥1 log 10 IU/ml 。 观察到最大降幅在第28周时为 1.65 log 10 IU/ml!乙肝表面抗原水平下降似乎与血浆ALG-001075的PK相关 , BID给药可能会进一步加强HBsAg的降低--队列计划 。
综上所述 , 该研究结论:在接受治疗的乙肝e抗原阳性受试者中 , 当与ETV联用长达28周时 , 表明ALG-000184通常具有良好安全状况 。 与单用ETV相比 , ALG-000184+ETV可导致HBVDNA下降幅度更大 , 可大幅调降乙肝表面抗原水平(高达1.65 log 10 IU/ml):在4/5名使用300毫克剂量 x ≥24周的受试者中 , 乙肝表面抗原下降 >1 log 10 IU/mL , 这种抗病毒效果似乎与活性药物的暴露有关 。
- 龙角散润喉糖| “全国都在嗓子疼”上热搜 龙角散好声音养护小课堂来帮忙
- 运动|“44岁以下算青年,60岁前都是中年”?现在开始做好抗衰老!
- 乙肝|乙肝Aligos制药更新,ALG-000184联合ETV,HBsAg调降高达1.65 log
- 减肥方法|如何逼自己在这个夏天瘦下来?暴瘦64斤的压箱底减肥方法
- 近视|叶黄素防近视是“智商税”吗?新研究:7类食物或可降低近视风险
- 运动|寿命“藏”在脸上?若您脸上有3个特征,说明身体硬朗,或能长寿
- 运动|最新研究报告表明:2035年全球将有超过一半的人口会变成“肥佬”
- 运动|怎样减肥最快?研究了999个案例,我总结了4个简单实用减肥小窍门
- 咽炎|全国都在“咽喉炎”?嗓子疼是“二阳”吗?解读来了
- 黑色素|压力过大会导致头发变白?新研究:白头发或许有望逆转成黑发?
