免疫|《科学》子刊:全球首个γδ T细胞抗体药物临床数据发布,新的免疫疗法即将诞生!( 二 )
图2:ICT01可特异性激活Vγ9Vδ2T细胞
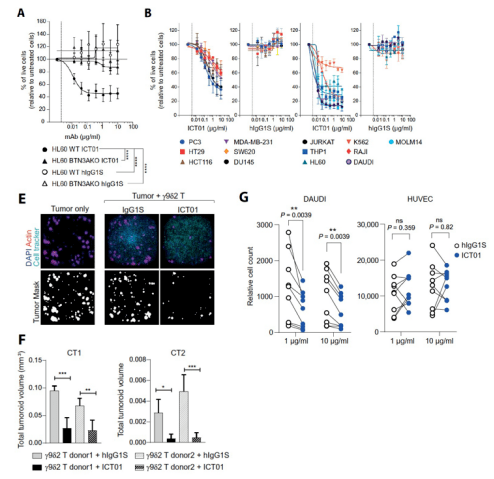
随后 , 研究者们进一步探究ICT01激活的Vγ9Vδ2T细胞对肿瘤细胞的杀伤能力 。 在包含白血病细胞HL60在内的14种不同肿瘤细胞的体外实验中 , 均证实了 ICT01干预后 , Vγ9Vδ2T细胞的激活可形成对肿瘤细胞强大的杀伤能力 , 且该杀伤过程依赖于BTN3A的表达(图3A-B) 。 此外 , 在大肠癌类器官3D模型中 , ICT01诱导的Vγ9Vδ2T细胞对肿瘤细胞的杀伤作用同样显著(图3E-F) 。
而以ICT01干预非肿瘤性人类脐静脉内皮细胞(HUVEC)时 , 尽管检测到了Vγ9Vδ2T细胞的数量增加 , 但HUVEC细胞的存活率并未受到影响 , 表明 ICT01诱导的Vγ9Vδ2T细胞的活化可特异性杀伤肿瘤细胞 , 而对正常细胞的存活无明显影响(图3G) 。
文章图片
图3:ICT01激活Vγ9Vδ2T细胞对肿瘤细胞的杀伤作用
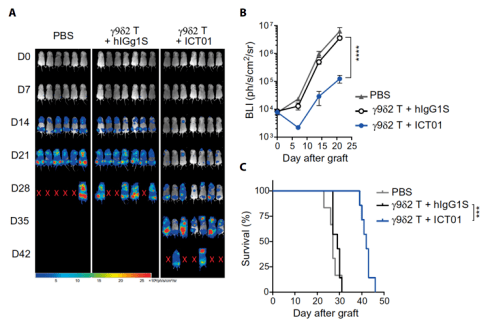
接下来 , 研究者还构建了NSG小鼠移植瘤模型 , 进一步证实ICT01通过激活Vγ9Vδ2T细胞发挥抑瘤作用 。 与对照组小鼠相比 ,γ9δ2T细胞+ICT01组小鼠的肿瘤生长明显减慢 , 且中位生存期由39天延长至42天(P<0.001)(图4) 。
文章图片
图4:ICT01介导Vγ9Vδ2T细胞抑制小鼠移植瘤的生长
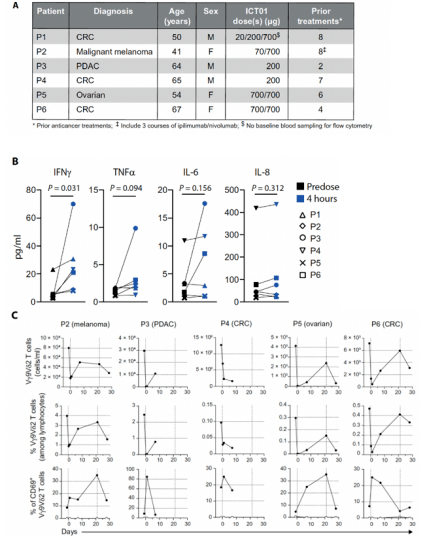
作为一种全新的人源性单克隆抗体 , ICT01在临床中应用的安全性及耐受性也得到了证实 。 在开展临床研究之前 , 研究者在非人灵长类动物体内开展一系列研究 , 在每周予以0-100mg/kg剂量ICT01的各个干预组中 , 均未观察到ICT01导致的动物死亡及其他不良反应 。
文章图片
图5:ICT01在进展期肿瘤患者中的临床研究
综上 , 研究者们研发了一种全新的人源性抗BTN3A抗体ICT01 , 可特异性增强Vγ9Vδ2T细胞对多种肿瘤的杀伤作用 。 ICT01能够以亚纳摩尔级别的亲和力和高度特异性与BTN3A 的3种同型异构体相结合 , 且不依赖于B30.2结构域 。 此外 , 动物实验及临床研究均在一定程度上证实了ICT01的安全性及有效性 。 总之 , 关于ICT01的研究成果目前仍是令人振奋的 , 其在抗肿瘤免疫治疗中的作价值还需要有更大规模的临床研究加以证实 。
参考文献:
1. Chien, Y.H., C. Meyer, and M. Bonneville, γδ T cells: first line of defense and beyond. Annu Rev Immunol, 2014. 32: p. 121-55.
2. Kabelitz, D., et al., Cancer immunotherapy with γδ T cells: many paths ahead of us. Cell Mol Immunol, 2020. 17(9): p. 925-939.
3. De Gassart, A., et al., Development of ICT01, a first-in-class, anti-BTN3A antibody for activating Vγ9Vδ2 T cell-mediated antitumor immune response. Sci Transl Med, 2021. 13(616): p. eabj0835.
4. Gentles, A.J., et al., The prognostic landscape of genes and infiltrating immune cells across human cancers. Nat Med, 2015. 21(8): p. 938-945.
5. Harly, C., et al., Key implication of CD277/butyrophilin-3 (BTN3A) in cellular stress sensing by a major human γδ T-cell subset. Blood, 2012. 120(11): p. 2269-79.
- 免疫|1碗抗癌汤消炎、抗氧化、强免疫!利用大白菜、菇类快速搞定
- 口味|给孩子做个“快手菜” 营养丰富,口味独特,提高身体的免疫力
- 卫生室|《乡村医生诊疗口袋书(先行本)》面世
- 鲁南制药集团|菏泽医学专科学校“鲁南制药产业学院”揭牌
- 收发|一图读懂 | 科学收取快递 做好健康防护
- 解读|《浙江省医院门诊管理办法》政策解读
- 孩子春节最爱的“香蠕菜”,提高免疫力、增强体质,更健康
- 孩子春节最爱“黄金菜”,补充营养,增强免疫力,身体更健康!
- 过年孩子必须要吃的美食,暖身暖胃、提高免疫力,冬天不生病
- 立冬后,孩子嘴馋的“高钙菜”,补充钙质,增强免疫力,不生病
